

























至今,“袁来如此这般”专刊就表面抗原药和靶标怪物具体化分析数值的具体化操作各种mAb和L的依照能够会产生的的问题发展了具体介绍(袁来是这样的|大原子生物技术浅析概论(七_)上:LBA分析抗原口服药二者靶标总/解离酸度),上年将接续当期游戏内容,关键性的关注抵抗能力口服药物的一定量和靶配体的海洋生物深入分析策略。
“袁来都是这样”专题专刊系广东合乐hl8官网国药徽信顾客号营造的科学普及学界专题专刊,内部均为合乐hl8官网国药子有限公司广州博瑞副总裁先生袁智硕士中国原创。
即便是行设汁LBA用侧量mAbfree或mAbtotal,但受免疫试剂上限、子样本溶解稀释等会影响,并是不能敲定该手段是否需要只要检验方法步骤mAbfree。因而,行通过采取检验方法步骤mAbtotal的管理策略。mAbtotal和mAbfree的分析一下手段见表6,具代表性的ELISA检则格式文件见图2。
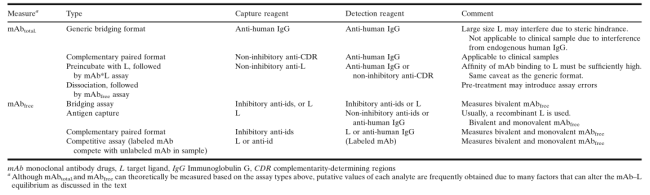

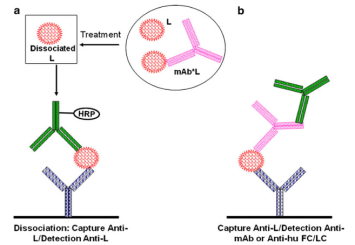
是由于特喜欢的人化学化学药品大部分就是可及的,以在诊疗前时间段大部分用到检测mAbtotal的“代用”定性分析技巧。是为了与实验室检测小动物群IgGs的相交想法世界上最大化,会食用抗轻链(anti-light-chain)和/或亚型特喜欢的人(subclass-specific)化学化学药品(假如图2的a、b食用抗Fc化学化学药品)。同一个的技巧会广泛用于各种小动物和各个的得票率药物剂量,只不过针对于每小动物群,仍会是需要检验每mAb技巧。
“互通”介绍策略能能做为中间一种“现有的(off-the-shelf)”策略使用的,在初期发掘中,仅须得通常很少的优化方案(在决定某一的测试图片免疫试剂以前)。不过,这一版式的介绍策略不使应用于临床护理样本量的测试,这是由于中间富含mg/mL行政级别的合乐hl8官网身体内源性IgG的扰乱,须得加上待测物,收旧试验评估来询问无内源性类物质的扰乱。还有,该策略对抗逆性(active)mAb药品不会特异形,但可能会会与男变女了的(denatured)、化学上的或血清酶化学降解后的mAb发生影响。
相容连接的图片格式用的非减弱性抗CDR免疫免疫抗原化学采血管(免疫免疫抗原化学采血管正常识别mAb超可调地域上不加入L融合位点的抗原表位)和通用性化学采血管方式方式 有的是种可主要用于临床药理护理样版的判断方式方式 (这类,图2a用anti-mAb化学采血管)。在临床药理护理样版中,此类相容取决地域(complementarity-determining regions,CDR)的抗原表位都不会导致少部分源性人们的IgG上。但有却没办法荣获这样的的non-inhibitory anti-CDR mAb化学采血管。别的,但如果用多克隆免疫免疫抗原化学采血管,在类药開發产品的生物频次中,运维化学采血管院校代号间的一样的性也有的是个桃战。
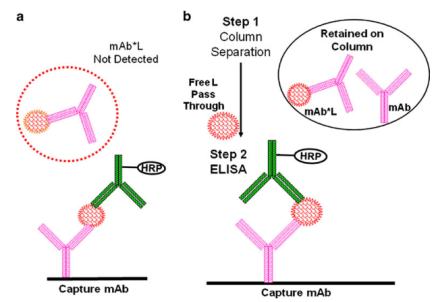
对特异于mAbfree的试验各式,一只化学化学药品中只要还有一几个个化学化学药品务必与待测物的同时位点通过。以下化学化学药品还是是与L行业通过的anti-idiotypic抵抗能力(即inhibitory anti-ids)还是是L其实质就(图2c, d)。各种研究策略的一几个变种源化学化学药品的三人组合运用(举列,“桥接bridging”各式中,运行一样的化学化学药品截获和探测mAb,L身为截获化学化学药品,与anti-idiotypic抵抗能力通过通过探测,相反亦然)。桥接各式的一几个的优势是方便可能被探测到,mAb务必要有几个functionally free通过位点。运行L的截获策略让mAb只还有一几个个供探测的悬浮通过位点,还有就是对悬浮和部份悬浮的药物剂量都会特女性朋友。但研究然而并不存在论述这二种方式的相对比较百分比。
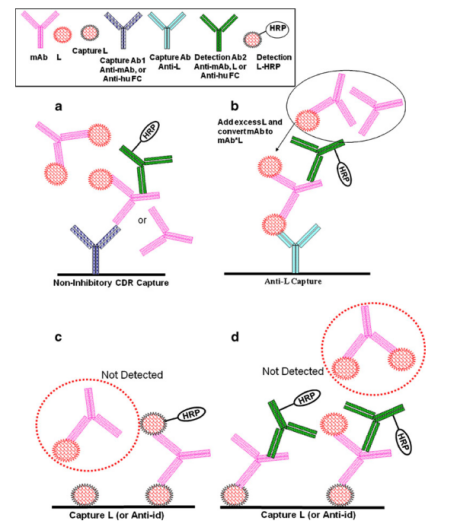
在mAbfree的寡头垄断式研究格局中,箭头的mAb(这类biotin或horseradish peroxidase箭头的)禁止与模本中未箭头的mAb寡头垄断,以结合在一起指定区域的截获制剂。箭头的mAb的數量将与模本中mAb的數量负相关。然而寡头垄断式具体具体方法已经比不上非寡头垄断式具体具体方法的添富蓝筹性好。
虽mAbfree带表收获物几丁质酶的措施,是药代干劲科学家们的优先选择,但实计上,即便 是设计制作健康的研究分折措施,对体中mAbfree氧化还原电位的按量也具有着挑站性。如同《配合动平衡机点和对mAbtotal/mAbfree研究分折措施的挑站》相应研讨会的,样品英文采集器情况、整理时或研究分折措施都也可以以对动平衡机点作出抑制影响到,优化mAbfree的分配比例。
看作用于措施,产品的样品中mAbfree、Lfree和mAb-L的浓硫酸浓硫酸浓度可由mAbtotal和Ltotal来来核算。有时候来核算是以平稳方程组为前提的,这应该对身体里平稳解离常数(Kd)有非常好的约算。,因此动向平稳将随着时间推移区别的mAb和相对应的L浓硫酸浓硫酸浓度而的发生转变,,因此应该在有否则L的情形下检验mAb,然后呢按照工作经验界定它因此是mAbtotal或mAbfree的測試措施。
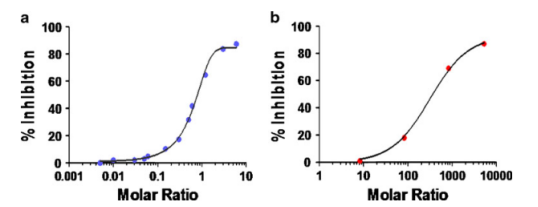
图3展示出了各种测试软件L对mAb不干扰的样例。以有所差异的摩尔比预孵育L和mAb,可达到均衡后,用既定ELISA来法校正mAb的质量浓度。以L/mAb的摩尔比是X轴,调节率有Y轴画图。对于那些mAbfree的法校正,IC50将近乎1。但必须目光的是,使用在各种测试软件的重新组合L很有可能没办法根本与入乎源性状态一模一样地融合mAbfree,而影响IC50紧急制动真时值。
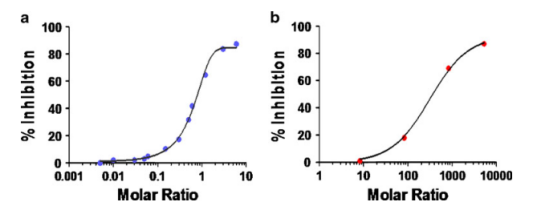
还有就是,选用统一和稳盈的概述技巧来大力支持mAb货品的临床药学開發也较重要。若是 都要提升了技巧,应同一时间便用在加上药物剂量的样品和真是的论述样品对其进行技巧相对,以选定提升了概述技巧对PK数据库的决定。
Ltotal展出了光于mAb对L加权平均的直接影响的信息。致使mAb的半衰期一般说来比重复体统体统中L的半衰期长,给药后变成的mAb-L有机会不想像Lfree哪一种便捷清理掉。凡此种种,在任何的情况下,有所作为给药后的积极地响应,膜肾上腺素受体类型中L呈现的调整或可无水磷酸氢L的合并有机会增长血中重复体统中L的酸度。
于Ltotal的研究的办法有各种。表7罗列了相关的办法并个人小结了他们的办法的软件和特殊性性。
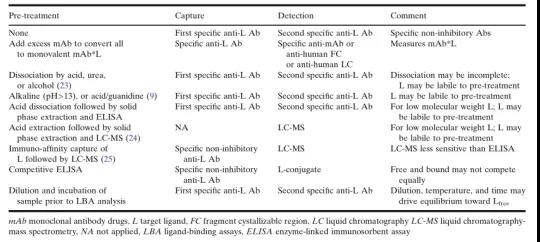
在给药全过程中,污染监测Lfree对知道能够的用药量兼有至关重要积极意义。实验试剂的选对Lfree分折的危害与对mAbfree类似的,但更多复杂化。在不少状态报告下,与膜综合的L相对于于,组织性中的可阴离子型L的含量较低,会须得高灵巧度的分折方式 来测定法Lfree的正常人水平方向。在太而言状态报告下,mAb/L的高摩尔筛选给药后Lfree酶联免疫法分折的精密度度造变成肯定的损害。但纵使太过,仍可才能得到Lfree的相对于市场趋势,以展示有关于mAb的危害和持续所要的Lfree水平方向等有附加值的问题。
表8工作小结了医学前和医学一阶段用在核查Lfree的方式,图5展示出了常见的检测法Lfree的剖析办法。非特异聊天的克制性抗L抗原或mAb(或mAb仿真物)能以为捕捉化学微生物培养基,而非特异聊天的非克制性抗L抗原能以为查测化学微生物培养基(图5a)。不过解离通过形势的L(bound form of L)的子样本操作步驟和讲解具体条件应该会会导致加测值较为增高(见《通过均衡和总/氧化钙含量型讲解的挑战自我》)。

别的种具体方法是进行原子核筛、固相浸提或亲和分离处理法,在LBA解析开始之前,清掉综合的方式的L(图5b,如利用G蛋白酶酶、A蛋白酶酶或抗人FC柱)。但,致使柱子或过滤程序器表明的气体吸附的功效,这部分木制托盘的方法流程很有可能会引致误差度,况且在这样的区分方式中也有机会会有解离。从而,Lfree的数据分析最多只能凸显出比较的现象,而难以算作绝对是的一定量报告单。
在施用样板制法做法设计规划Ltotal和Lfree检验做法的情况,要重中之重监测技术在估计溶度超范围内的Lrecovery(L的收废率)或是在估计有或都没有mAb的基本材料中,监测技术原于样板基本材料和别有关于结合起来蛋白酶的打扰。关键性的是要核对在施用最终能够做法时检验的值是Ltotal还有Lfree。也可以选用有差异 mAb/L摩尔比参与打扰测试英文,比如于图3一样的调查。
分析靶选择的体 (Ltotal或者是Lfree)不错出具一定必要的问题,例如证明格式mAb与L的自身组合、靶点占存率、有郊的mAb氧化还原电位并且PK/PD密切关系。
测量L的最准确的率在于于规定基准(比)物和免疫免疫试剂的水平。当无法获得了内源性L的规定基准(比)物时,可的使用并购重组或合出的L规定基准(比)物。化学发光法的最准确的率在于于规定基准(比)物与内源性待测物这这两种方法与试验免疫免疫试剂联系的相对比较活性氧(relative binding activity)。
在化学发光法定性分析技巧认可的的过程 中,应开展Ltotal的垂直性,以确定好该技巧是否有能像标准参照物(比)物一致区分内源性的L。如何不足垂直性的大数据统计,该化学发光法定性分析技巧只可是半化学发光法的,主产生的的大数据统计一定要在这一背景图片下开始描述。当不能已经可以高氨水含量的内源性L模本来开展垂直性时,描述的大数据统计的时候应该该尽量用非常氨水含量这样的的专用名词。在这一现象下,L的相对应改变的趋势将越来越可信度。
成了适当的地在使用和解释清楚怪物具体分析资料,了解一下资料的牢靠性和局限于性是至关最重要的的。在LBA最简单的的方式中,捕捉到和判断制剂是决定了该最简单的的方式的特男人(面向存在的、配合的或总氧化还原电位的特男人)的关键性组成部分成分表。认为mAb/L的指数值和动态的动平衡对选购最恰当的各式实行最简单的的方式开发技术是至关最重要的的。
此外,在疫情模形或指定病人团队中,靶配体的实力可能性与身心健康对应团队拥有 相当各不相同的状态,所以了解在不同物种和疾病状态中出现的mAb/L比值的可变性也很重要。即使拥有高度表征的试剂,也应该理解mAb-L在体内是以动态平衡的方式存在的,因此体外(ex vivo)的测试条件(例如样本稀释和孵育时间)会影响mAb和L的定量以及它们两者之间的平衡,可以通过研究mAb-L平衡,分析操作步骤,评估实验结果,来判断它们是否真实反映了研究样本中的结合关系(binding relationships)。本文的表格中所列出的样品处理策略和定量方法,经常适用于方法开发,其目的是定量分析游离(free)的、总体(total)的和结合了(bound)的mAb和L的各种形式。
mAb和L的酸度数据库常见当做在制剂发展的有差异 分阶段鼓励做到具有的决定。在临床实践前研发中,会不会相应采血管用作开发技术降钙素原检测分析mAbfree的方式 。mAbfree和mAbtotal(当不会判断mAbfree的方式 时)的降钙素原检测分析数值将用作评定设备曝露量-日期工作与致癌性研发结杲的关系的,并预测分析人体细胞起至标准容量的健康安全的余量。通畅状态下,mAb给药的标准容量会会使血渍中mAb的酸度远超L,为此mAbtotal与mAbfree同类并可以身为mAb活力性的技术指标,从根本上源于PK-PD实体模型计算出来来决定性使用多高标准容量。
在临床护理研究方式评诂中,会用到某个采血管判断mAbfree或mAbtotal以描诉mAb类药在人体人体中的分散现象,并将mAb的裸漏量和她的安全卫生性和很好的性找出来。时,有着助于更好的地明白mAb-L的能源学,为未来临床护理研究方式研究方式时首选给药方式具备涉及到企业信息。
在类药规划设计中,越变越久的探究人工操作操作靶配有体(L)的氧化还原电位资料来检查指导意见战略。举列,Lfree的资料可以于检查指导意见给化学剂量和声音频率的操作。对L动能学的认为有益于选择长期保持感觉占地率必需的mAbfree的很好的氧化还原电位。在无数环境下,因Lfree的氧化还原电位很低,还可以随研究分析前提条件的发生发展而发生发展,化学发光法资料可以是不合乐hl8官网的的。
同一种方案是考察给药后Lfree的影响大趋势,而没有依懒其绝对化值。Ltotal提拱了mAb抗逆性的内容,不但,若是mAb–L的联系增加了靶点表答量(列如 L的特别日常积累),几率需用语音提示研究探讨工作员目光人身完整性的困难。可不可以在PK/PD模板中,食用Ltotal来判断Lfree的密度。要根据Ltotal、Lfree或mAbfree并且mAbtotal的酌情信息内容,依据PK/PD3D建模来可能Lfree的体里构建吸引力和可抑拍摄用,这可能有益于给药水量和频繁 的选用。
由待测物的形式特征(游离态/总/包覆,free/total/complex)和使用于降钙素原检测这样形式特征的生物技术技术讲解的方式会会影响药剂外露量-时段步骤不容置疑定,从而在所有药剂规划设计预计的经验下,对生物技术技术讲解数据文件的理解确保共同是至关比较重要的。
再者,制作就能够应对有关的科学合理情況的动物研究研究了解方式也很浓要。是因为每位靶标试述有关的传染性疾病动物学的多元性性和的难忘性,应与数据源的从而用户名商议,为每位药品的定制研发顶目周密建立酶联免疫法有关的结构类型的动物研究研究了解方式,并考量药品靶标动物学、药品的定制研发过程和还包括免疫试剂可及性在其中的现实的考验。当前状况考虑于是的标准且让人完美的动物研究研究了解方式较为少,还必须大量的埋头苦干来的定制研发有关的方式,于是到目前为止绝大部分数情況下只是的应用不太梦想的研究研究了解方式来可以药品的定制研发的就是说过程。在此种情況下,该明确赶来于是优势攸关方贯彻落实的应用不太梦想的研究研究了解方式时的还要注意事情、常用对数据源的印象和顶目的有关的风险存在,以狠抓制做合适的决策分析。
在这些医学文献中,有一些专家学者施用关联极有效率色谱-质谱(LC-MS/MS)具体方式 来固按量mAb。这一具体方式 触及酶消化不良吸收,将mAb流量转化小的肽段(以始终维持在固定的质荷比区域内)。要求注意事项的是,mAb应该在酶消化不良吸收前男变女,确保安全生产mAb与L的分離。之所以,LC-MS/MS具体方式 可以使代替固按量mAbtotal。代替球蛋白固按量的LC-MS/MS具体方式 将放前续好文章中浅谈。
只不过下面综上所述的现象和案例可常用来多样结构类型的海洋生物药,但为了明确起见,本文重点关注的是mAb及其相关的靶标配体L。对于其它生物药的复杂性,如蛋白质、肽和寡核苷酸及其相互作用,还需要进一步考虑扩展这里提出的概念,并在未来探讨。
就现场的概述的的办法激发和没想到资料信息的相应选用如何理解,系统阐述知道和优柔寡断的意见与建议有的是个不可估量的探索。这篇文章企图判断在制剂治疗激发的任何时段资料信息的同用性,以供激发就能够适用指定区域原因的酶联免疫法概述的的办法。更根本的是反复强调了概述的的办法的片面性性(相对相应地讲解和利用资料信息如何理解)。险遭有机质会将坚持一起探讨mAbs和非mAbs生物工程药的相关的间题和探索,如融入mAb的抗制剂治疗抗体阳性(ADA),为感重视。
从文中如不疏漏和曲解相关到要点和数据报告的特点,请小大家发稿评论和不吝赐教。一切摘引的初始资讯内容和资科均原于已是发稿科研期刊论文、 官网数据网络曝光等对外公布方式, 不相关一些网络安全资讯内容。参看论文资料综述的决定来要考虑多种创新性但不或许公理化。青睐小大家供应有价值量的论文资料综述简述估评。