

























上周四,“袁来是这样”栏目就肿瘤药物发展全过程中是怎样解决或消减对LBA酶联免疫法浅析步骤打扰的营销策略进行了祥细介召(袁来如此这般|大动物大分子动物分折概论(六)上:LBA降钙素原检测抗原药剂的背静扰乱以及削除),小编将续展下期玩法,核心特别关注表面抗原生物工程药的按量定量分析。
“袁来如此这般”特刊系长沙合乐hl8官网生物医药资子公司微商媒体号创建的简单讲解学术界特刊,主要内容均为合乐hl8官网生物医药资子公司子资子公司广州博瑞副总先生先生袁智院士创作者。
LBA测验手段长用于参考值怪物机质中免疫抵抗能力中药的质量溶度,通过测验各式的各个,LBA能够 测定法徘徊子中药的质量溶度或中药总数。徘徊子中药是不与靶点融入在一起的制疗性免疫抵抗能力。中药总数则指徘徊子的加融入在一起了靶标签中药。可能PK参数至关关键性,关联风险防控要点和业内有目共睹都对参考值手段的效验提出了了关联提议,例如规避电磁干扰的有些的方面。
游离的抗体药物的测定通常使用抗原或中和性抗独特型抗体(anti-ID)作为捕获抗体。检测抗体可以是中和性anti-ID、非中和性anti-ID、抗人IgG、抗人特定等型(specific isotype)抗体(如抗人IgG2特异性抗体)或抗药物抗体的框架突变(anti-framework mutations)的抗体。抗体药物总量可被非中和性anti-ID、抗人IgG、抗人特定等型(specific isotype)抗体或抗药物抗体的框架突变的抗体捕获和检测。但是,很少能得到非中和性anti-IDs,因为在大多数情况下,生孩子anti-IDs时会产生很多中和性anti-IDs,但非中和性anti-IDs的产生量却很少。
悬浮抗体阳性药材的定量分析在技術上是具有着探索性的,特别是当可无水磷酸氢靶标在范例中长期处在高层次时,多个栽培基质组分是可以可观变化无常可无水磷酸氢靶商标层次或直接影响药材与可无水磷酸氢靶商标根据,最后引发悬浮药材浓硫酸浓度的变化无常。不仅如此,一些组分也很有也许对前面所议论的可无水磷酸氢靶校准量分析发挥干扰信号。
在定量解析解析抗原-口服药偶联物(ADCs)时,样版的准备具备着非常规目的意义,正是因为ADCs可以在采集工具的样版中或肚子里会发生怪物被转化,使本已缜密的ADC怪物解析变得更加缜密化。
既然是单克隆抵抗能力阳性的化学发光法也会得到样例制作形式的危害。譬如,施用EDTA用作抗凝剂会螯合阳亚铁阴离子(如Ca2+和Mg2+),关键在于危害分离抵抗能力阳性药材氨水浓度的精确检测法,如果你等阳亚铁阴离子是药材与靶标通过所必需品的。
在样例征集和化学合成的时候中,不理想化的程序代码(如上半篇说起的生物学符号物大部分所座谈会的)会从肿瘤细胞中发出可无水磷酸氢靶标,导至样例中靶标签有机废气氧浓度人力地增加,以此低估了游走抗体阳性的有机废气氧浓度。
要降低这么多潜在的的干拢,在对每一个抵抗能力制剂开始解析时,都会优化调整样表获取系统和查测水平。然而上面所涉及的,提纯血清的时可挥发储藏在血小板计数中的核蛋白质含量质含量,而运行血浆则可避免出现它的挥发。不仅而且,能能推进样表增稳的水平,如超低温,能能降低在样表回收时中核蛋白质含量质含量从内部中挥发出的量。在查测实验试剂产生的现状下先开始样表酸解治疗,再开始与治疗,或在查测时中保持稳定样表的强含酸性,该办法已被证明怎么写能能合理有效地降低出于靶标底干拢。
相对于悬浮抵抗能力口服药的了解,须得推广检则能力,如孵育时刻、捕捉化学试剂的氧化还原电位和保底做好稀释工作液的要求,以最多幅度地限制口服药从它的靶标解离。这对与它靶标判断力较低、在动脉血再循环中可无水磷酸氢靶标氧化还原电位较高的抵抗能力口服药,甚为本要。于是,想要在探索群体中评估报告做好稀释工作液线性网络度和子样本不稳化学发光法分析性,以将靶标技术的发生变化对悬浮口服药化学发光法的为准性某一决定定为注重。
当用到抗原捕捉待测物时,高含量的结合起来蛋清或可可溶性蛋白激酶(soluble receptor)机会会饱满捕捉实验采血管,招致游离于食用的药材的含量被低估。用到结合性anti-ID,而就不是食用的药材靶标,看作捕捉实验采血管,则就可以极限局限性的可以减少这是间题。
范例中的ADA是产品扰乱的一家源头。ADA与采集免疫抗原阳性(或在均相各种测试技术中的查测免疫抗原阳性),结合在一起到免疫抗原阳性药上,这个争夺会低估免疫抗原阳性药的渗透压;非争夺性ADA能令免疫抗原阳性药分子式交连导致基本量的组合物,这也会会影响药渗透压核查的精确性。利用对PK、PD和ADA的结论来比效,可查验探索中有没现实存在这个扰乱,而一定地表示相关数据源。
与生物学标注物旋光度的测定相仿,产品中的heterophilic抵抗能力阳性两个人抗爬行动物抵抗能力阳性是免疫检测判断判断中的比较常见反应电磁波源头,还能够用所诉想同的具体方法来缓解反应电磁波的反应。如若利用抗人抵抗能力阳性充当采集或检判断剂,身休产品中的身休免疫检测判断球球蛋白可出现不错的背景图案电磁波,还能够首选利用Isotype-specific anti-human antibody取代pan anti-human antibody,以下降反应电磁波。
生物制品药和基本的人源抵抗能力药都有着很有可能诞生ADA(也是指抗药抵抗能力),会使得药爆漏量的亏损资金、疗效亏损资金和厉害的不合格品反映。抗体原性进行分析评估报告是临床试验调查中安会性进行分析评估报告的关键組成大部分,ADA一般说来运用级别划分的的办法完成在线探测(基因探测)、证实和定性进行分析。ADA法测定是半一定量的,毕竟许多检查的的办法缺乏性细则弧度。呈阳性的基本概念是在检查切点上述的在线探测数据信号,由未接手药的阴性化样品的数据汇总进行分析认定。
重要性抵抗能力药ADA的剖析也注意是能够LBA最简单的技巧做好的。大多都数ADA抗体阳性细胞剖析利用桥接试验各式,即ADA桥接(bridge)/化学交联(crosslink)好几个治疗药物分子式配合。对抵抗能力药中安全使用较少的另种最简单的技巧是会直接配合抗体阳性细胞试验(direct binding immunoassays),在这当中抵抗能力药是猎取微生物培养基,检试验剂则是监测ADA的Fc一部分。
在ADA检侧中里通常的要素是抵抗学习能力药自身,样例中的制剂与ADA融入,放到ADA与检验化学药品组成符合物,在制剂存在的的问题下检侧到ADA的学习能力,又称制剂耐药肺结核性。
在临床药学药学和非临床药学药学ADA耐压试验步骤效验的过程 中,行业管理医疗机构会耍求评价和除掉是这样的侵扰,就能够开展在肿瘤药剂溶液浓度预期目标较低的时段点(drug wash-out phase)分类整理范本开展ADA软件测试来控制肿瘤药剂侵扰。在一些情況下,开展酸分开就能够从而提高肿瘤药剂承受性。
(1)安全使用酸解离口服药物-ADA黏结物;
(2)在加测化学药品的存有的问题下与样品;
(3)通过自测
应用高迅敏度的剖析方式手段和稀释溶液范本是提升抗药理作用的有效的方式手段,类药剂驯服ADA并进行Fc部位测量ADA的直接的紧密联系式LBA方式手段或者较少由于类药干拢,在类似这些方式手段中,但凡ADA的左端可与类药驯服紧密联系,就能测量到ADA。
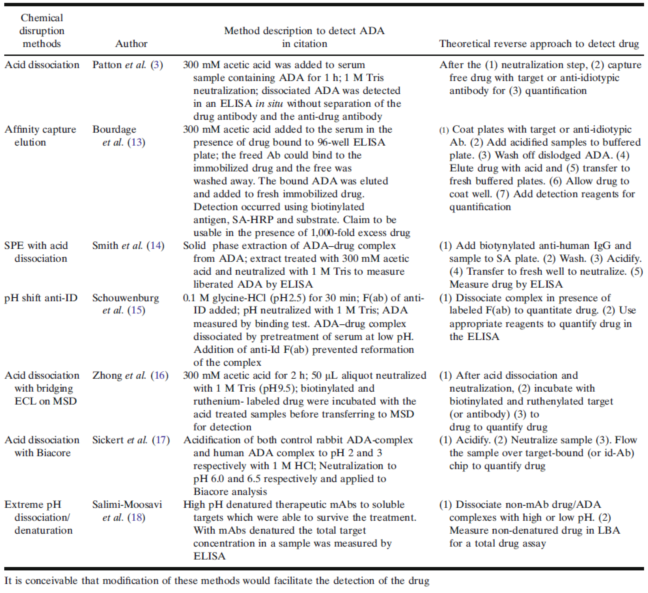
桥接的测验论文格式则规范要求ADA的两端融入到测验微生物培养基,Wu几人表述半个个间接融入式,以测试中成药特女性朋友的ADAs(IgE等型),并会通过提纯抗体阳性量总数量,随之测试copurified 中成药来酶联免疫法ADA,也许会全消失中成药骚扰。Neubert几人经过protein G extraction,再采用LC-MS检验copurified中成药,说明了此方式的准许性。表1 找出来半个些用到损伤ADA-药物治疗符合物,以提升 ADA检验敏锐度的方式(具体情况见扩大仔细阅读#2)。局限于通篇,这篇不相信依次小组讨论,请参阅这篇末的基准论文。
样表量基本材料中的用药靶标也将会不侵扰ADA加测,会造成假阳型或弱阳性反应毕竟,桥接抓取和加测化学药品的multimeric可无水磷酸氢靶标才能生成假阳型毕竟。有报道怎么写称,在ADA各种测试中,包含的CD20的内部膜情节会对atumumab生成基本材料不侵扰,弱阳性反应毕竟将会是是由于可无水磷酸氢靶标与抓取和/或加测抵抗能力依照,关键在于中医与性ADA的加测。接下来的样表量预工作,即用中医性抵抗能力依照靶标,或用依照球蛋白对靶标做出中医及免疫检测总量靶标,都能以解除这些不侵扰。比如说,在针对于ranibizumab的ADA方案设计规划的时候中取得了否认。
一般,通常数史学家表示未健康使用生物工程药的自己不就是有ADA,但时常在给药前就是监测到此前来源于的抵抗能力。适合一提的是,此前来源于的抵抗能力并不会是骚扰,且已经切合到抵抗能力性用量的很多地方。这类,监测到并明确了对panitumumab的与性ADA,但报导说这一些交错式作用性抵抗能力不曾调整性用量PK或其健康性。
哪怕太过,仍然的ADA有时候促使软件检测和最终解释一下愈来愈更僵化。滴度和特女性朋友软件检测有益于熟知仍然具有的抵抗能力对给药后ADA遭受率的奉献,争对cetuximab的仍然具有的抵抗能力有临床实践药理一些性,即仍然具有的IgE抵抗能力与造成 的超敏化学反应关以。当许多 抵抗能力类药包含有许多 非天然血清的天然免疫原性成分域有时大部分数人早先机会触碰到该成分域时,就很机会会要预先具有的ADAs。在recombinant therapeutic immunotoxins,即anti-CD3-diptheria toxin 和anti-CD22 Pseudomonas exotoxin A的临床实践药理理论研究中,就观查到仍然具有的ADA。
表1. 中用摧毁ADA-食用的药物复合型物,以提供ADA验测敏感度的方法步骤
在类痛风骨痛膝盖炎的人中相对比较比较普遍的类痛风骨痛分子(rheumatoid factor,RF),它是而对IgG的Fc区域环境的抵抗能力,主要的为IgM等型抵抗能力。RF的通过沟通协调能力低,预期想象不已经在ADA测试英文中形成呈抵抗能力阳型警报,不过建筑工程更新过的抵抗能力口服药剂量已经对RF有更大的沟通协调能力,以此已经在ADA检验中形成呈抵抗能力阳型警报。Araujo宋江因表明,在给药前的样表量中,RF形成了呈抵抗能力阳型警报,而动用抗人IgM抵抗能力的样表量特征提取会降低RF的角色。这样的方法已经会导致IgM等型的ADA检验,作家筛选了包带有和不包带有抗IgM抵抗能力的样表量,并监控口服药剂量疗法当天滴度的加强。
可溶解性淀粉酶海洋物理学体圆形标志物、改善性免疫抗体和ADA的海洋物理学体阐述是抗癫痫药物开发建设中不能够分开的一本分,每个种阐述物皆有其企业的挑战。防止基本材料串扰最更好的最简单的技巧是对靶标海洋物理学体学和待测物身还具有坚实的学说根本,并特别关注度测试仪/阐述最简单的技巧的特男人。
研究方法也几率在以免或限制考试骚扰方便树立必要用途。在一大堆的情况下,溶解是限制骚扰的可行专用生产工具,而最高的人的溶解度数受到了检测生产工具精确度度的限制。高精确度度的研究机构在高溶解前提条件下,能够带来可行的专用生产工具,以时应限制根据栽培基质的骚扰,提取和纯化方法的改变能够可行地将待测物从骚扰因素中提取出现。随后,在ADA研究中,可行地从免疫抗体用药-ADA挽回物中一定量提取出ADA就能完成其用药耐热性话题。
MS与LC根据以及成為一类强悍的化学发光法方式,还愈来愈群体越多的应运在蛋白酶药剂 (更是要格外重视是抗原药剂偶联物)和微怪物标志牌物的微怪物具体分折上。与LBA方式不同之处较,干拢对它的或许不这样最重要,鉴于MS是特情人好强的具体分折方式。固然具体分折特情人在齐全性去掉干拢的方面会极为有帮助到,但如果你待测物在微怪物学上是齐全性一样的(identical),它也应该使微怪物具体分折越来越及其繁杂。
在成千上万情况下下,MS要能查测成千上万差异待测物的相溶物,而LBA的方式只有查测一类待测物。故此,LC-MS/MS在微生态学进行浅析中挥发很越注重的能力。本产品以后内容将价绍分子式微生态学进行浅析中LC-MS/MS的方式。欢迎加关注。
从文中如果有疏漏和片面性涵盖到的手册和大数据的特点,请朋友平论和不吝赐教。全部使用的原问题和档案资料均根据都说出科研杂志, 管方系统报道范文, 等公开化推广方式, 不涵盖什么保密工作问题。参考选取文章的选考虑一下到各种各样化但是不或者有序性。青睐朋友给出有价值量的文章下列关于评定。
1. Schwickart M, et al. Interference in immunoassays to support therapeutic antibody development in preclinical and clinical studies. Bioanalysis (2014) 6(14), 1939–1951
2. DeSilva B, et al. Recommendations for the bioanalytical method validation of ligand-binding assays to support pharmacokinetic assessments of macromolecules. Pharm Res. 2003;20(11):1885–900.
3. Kroll MH, Elin RJ. Interference with clinical laboratory analyses. Clin. Chem. 40(11 Pt 1), 1996–2005 (1994).
4. Tate J, Ward G. Interferences in immunoassay. Clin. Biochem. Rev. 25(2), 105–120 (2004).
5. Weber TH, et al. Endogenous interference in immunoassays in clinical chemistry. A review. Scand. J. Clin. Lab. Invest. Suppl. 201, 77–82 (1990).
6. Levinson SS, et al. Towards a better understanding of heterophile (and the like) antibody interference with modern immunoassays. Clin. Chim. Acta 325(1–2), 1–15 (2002).
7. Kricka LJ. Human anti-animal antibody interferences in immunological assays. Clin. Chem. 45(7), 942–956 (1999).
8. Bolstad N, et al. Heterophilic antibody interference in commercial immunoassays; a screening study using paired native and pre-blocked sera. Clin. Chem. Lab.Med. 49(12), 2001–2006 (2011).
9. Stevenson LF, et al. Parallelism: considerations for the development, validation and implementation of PK and biomarker ligand-binding assays. Bioanalysis 6(2),185–198 (2014).
10. Lee JW, et al. Fit-for-purpose method development and validation for successful biomarker measurement. Pharm. Res. 23(2), 312–328 (2006).
11. Emerson JF, et al. Screening for interference in immunoassays. Clin. Chem. 49(7), 1163–1169 (2003).
12. Dimeski G. Interference testing. Clin. Biochem. Rev. 29(Suppl. 1), S43–S48 (2008).
13. Muller W, et al. Interference of IgM rheumatoid factor with nephelometric C-reactive protein determinations. J. Immunol. Methods 80(1), 77–90 (1985).
14. Kelly MM, et al. Increased detection of interleukin-5 in sputum by addition of protease inhibitors. Eur. Respir. J. 18(4), 685–691 (2001).
15. Salimi-Moosavi H, et al. Novel approaches using alkaline or acid/guanidine treatment to eliminate therapeutic antibody interference in the measurement of total target ligand. J. Pharm. Biomed. Anal.51(5), 1128–1133 (2010).
16. DeSilva B, et al. 2012 white paper on recent issues in bioanalysis and alignment of multiple guidelines. Bioanalysis 4(18), 2213–2226 (2012).
17. Partridge MA, et al. Minimizing target interference in PK immunoassays: new approaches for low pH-sample treatment. Bioanalysis 5(15), 1897–1910 (2013).
18. Verch T, et al. Pharmacokinetic immunoassay methods in the presence of soluble target. J. Immunol. Methods 361(1–2), 75–81 (2010).
19. Koren E, et al. Recommendations on risk-based strategies for detection and characterization of antibodies against biotechnology products. J. Immunol. Methods 333(1–2), 1–9 (2008).
20. Stubenrauch K, et al. Generic anti-drug antibody assay with drug tolerance in serum samples from mice exposed to human antibodies. Anal.Biochem. 430(2), 193–199 (2012).
21. Patton A, et al. An acid dissociation bridging ELISA for detection of antibodies directed against therapeutic proteins in the presence of antigen. J. Immunol. Methods 304(1–2), 189–195 (2005).
22. Zhong ZD, et al. Identification and inhibition of drug target interference in immunogenicity assays. J. Immunol. Methods 355(1–2), 21–28 (2010).
23. Xue L, Rup B. Evaluation of pre-existing antibody presence as a risk factor for post-treatment anti-drug antibody induction: analysis of human clinical study data for multiple biotherapeutics. AAPS J. 15(3), 893–896 (2013).
24. Chung CH, et al. Cetuximab induced anaphylaxis and IgE specific for galactose-alpha-1,3-galactose. N. Engl. J. Med. 358(11), 1109–1117 (2008).
25. Kelley, M, et al., Theoretical considerations and practical approaches to address the effect of anti-drug antibody (ADA) on quantification of biotherapeutics in circulation. AAPS J, 2013. 15(3): p. 646-58.