

























本段为分子结构结构生物体讲解概论类别内容的五、篇,主要说明LBA的办法的相水平性(parallelism)进行调查或论述浅析,这时分子结构结构用药讲解的办法所独特的问题论述浅析。相水平性是考核配体结合起来式测试英文的办法(ligand-binding assay,LBA)对于精确性的重点进行调查。
在这类的研究中,将运用含量线性的研究,即采用评诂报告格式扑灭对生态学机质中内源性待测物按量定量分析一下的反应,来解释的定量分析一下工艺的相应精准的性,可能评诂报告格式的大致特征描述是指确定性、机质定律、营养的最高扑灭4的倍数、建康和身患该疾消费群体的内源性待测物的含量及及LLOQ。文中将相对比较并热议评诂报告格式搭载PK按量定量分析一下定量分析一下的LBA工艺中核心参数表的指导意见工艺及及每款工艺的优优点和缺点。
LBA酶联天然免疫法研究措施,是能够比之比类药盐氨水密度的效准品各自不同盐氨水密度的怪物工程模本的天然免疫发生反应亲水性(immunoreactivity)来测得怪物工程模本广州中山大学碳原子类药的盐氨水密度。对於1个安全性能很好的LBA措施,其效准等值线(适于的logistic regression线性拟合的结果)应拥有垂直性,即才可以帮助有以下几点假如说:作考试化学制剂的抗原其组合功能充分相仿、可以用于检验掺水了的样品中的待测物的盐浓度。致使非平行线性的一个包括影响因素是:(1)进行校正定义(比)物料与不明待测物左右的免疫力吸引力的特点的性别性别差异(对截获和检查测量实验试剂所说);(2)进行校正弧线栽培栽培栽培机质、重量把控好检样(QC)栽培栽培栽培机质和学习三高人群的栽培栽培栽培机质左右栽培栽培栽培机质滞后效应的性别性别差异(图1)。
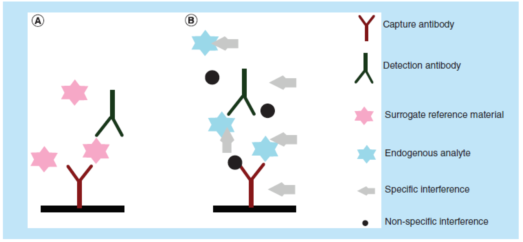
这对目的在于旋光度的测定外源性淀粉酶性药物以大力可以支持药代能量学(PK)探析的LBA形式,定义(比)规则物料一般而言能到仔细的研究工艺,且具备有进一步的深入分折证件(CoA)。做为复位品的定义(比)规则物料一般而言与待测物差不多。外部不一样的含量的待测物备制的效果管理试品则常见使用在评价指标精准的度、精硬度、选泽性、迟钝度和稀释溶液曲线度,以大力可以支持结果的一参考值深入分折形式的认可。新加坡FDA规程草案、EMA规程和互联网行业的共识发展报告仔细阐述了展开等等实验报告的有关的提议。当今,等等提议在常见使用在PK一参考值深入分折的LBA形式认可中已到常见地借助。
这对于检测内源性核蛋白质含量,如生态学标签物(biomarker)和“解离”/“总”用药靶标签LBA的方式的开发设计和认证证书,有关的原则将有差异 于PK降钙素原检测分析一下的方式。这是正因为常常不存有纯化了的、是表现的内源性定义(比)物,且包含待测物的空白图片栽培基质可能是不存有,故需的一种相对性降钙素原检测的的方式。应用于内源性待测物如生物制品标记物的LBA的方式的平行线性将朝后续篇文章中作专做研讨,拔冗私信。
总现阶段之,垂直性探索是依据剖析评估的办法扑灭对动物栽培栽培基质中待测物化学发光法阐述的决定,来表现是一个阐述的办法相比精确性性(relative accuracy)的每项主要指标图。行剖析评估的办法的有关阐述的办法的大致显著特点属于的条件性、栽培栽培基质滞后效应、所须评均扑灭公倍数(minimum required dilution, MRD)、卫生和患有客户群体中内源性待测物的氧浓度和LLOQ。
在往日的十来年中呢,,完美学术论文中就成平行线性实验设计的操作和用于标准化公布了众多座谈会报告。200四年,DeSilva等等提倡应用由些Cmax模板(已测模板再定性分析模板)制造而成的混杂模板,以能够PK工艺的调查中认证。2011EMA手册可以施用高含量探讨样例(Cmax探讨样例)溶解稀释到最少以下三个含量来鉴定PK方式的相平行性,还意见计算的直接稀释就可以范本之中的精比热容以评估报告相垂直性。是由于安全使用了真實范本对其进行相垂直性实验探讨,即实验探讨范本中的待测物就已经 出于生物体技术产品中,而如果不是另外待测物到空白页生物体技术产品而行成实验探讨范本。
如此,在多种实际意义上采用作PK化学发光法酶联免疫法深入分析的和用作生物学标志logo物的LBA技巧在直线线性研发中仍处于相近认知度。那么,似乎选文预期的只热议用作PK化学发光法酶联免疫法深入分析的LBA技巧的直线线性,但下部的热议往往会也提及或比效矛盾律。
中心句将浅谈并更有关于评估报告关键性技术指标的工艺,是指倾斜角性进行实验和各种传统型的工艺,讨论稿怎样才能用到倾斜角性统计资料来专业指导数据分析工艺的开拓或每一种攻略的优弊端。
LBA化学发光法判断有于动物制品机质中的待测物,需事后浸提。在比较好情形下,捕捉/测量工具采血管应搭配(还有就是仅搭配)待测物,切实保障其并不会与一切以外的别的的蛋清发生重叠反映。没想到的是,情形恰恰并不一定那么。在显示世间中,动物制品机质中的内源性蛋清时不时阻挡采血管与待测物的搭配。内源机质电磁波辐射物能能活性聊天地或不是活性聊天地搭配捕捉/测量工具采血管或待测物,可使测验预警不断增加或削减。
一般说来用的非特女性朋友电磁要素是基于溶血(hemolysis)、脂肪酸血症(lipemia)、抗凝剂(anticoagulant)或其余小原子有机酸或三聚氰胺树脂物品的主动效用造的。对PK一定量最简单的方法的特女性朋友电磁要素将来自五湖四海淀粉酶酶抗癫痫抗癫痫药物的可降解副产物、内源淀粉酶酶的相似物、异质性抗原(heterophilic antibody)、人抗各种动物抗原、风湿骨痛因素、可溶解性配体、抗抗癫痫抗癫痫药物抗原、高使用量钩不确定性(high-dose hook effect)等。在存在的电磁要素物一般说来都没有研究方法优秀的基准(比)物需用,并且一般说来不晓道电磁要素物的化学性质,而有尚未马上测试软件全部存在电磁要素物。
过去上,会在方式设计第一阶段采用再加上待测物/回收处理率测试来考评机质边际反应。如何制作准则申请这类卡种弧度提额的机质与范例机质相等(列举与基本都数PK降钙素原加测方式一样),则任何事物的机质边际反应一般说来相拟。seo机质的选购更高是要上升迅敏度(sensitivity),而不上升最准度(absolute accuracy)。而言基本都数需用换用机质的测得内源性待测物的LBA方式,需用安全选择换用机质所制作的准则申请这类卡种弧度提额,算overspiked matrix control samples中待测物的密度,以考评根本最准度。只是,前一自然的没字机质不了迅速,则需特意仔细。犹豫自然机质中的内源性待测物的密度是安全选择换用机质的准则申请这类卡种弧度提额被测得的,故此不了以确保这些测得后果的根本最准度,这个是犹豫因素的机质边际反应差距和因素的加测方式迅敏度的要求。
形成直线线规则化实验性能助认知该分折技术的相比明确性(relative accuracy)。真是在生成测量仪移动信号与做好掺水工作4的倍数或浓硫酸浓度的关心图,以评估报告报告相比误差,而使评估报告报告该技术的机质效果。操作原有数据报告有多种不同的的技术。这个技术将在"形成直线线规则化、做好掺水工作规则化和选定性"的章节内容中研讨。4个样品的结果英文直线理应反馈了测量仪实验试剂待遇测物和机质干涉物的综合管理亲和(combined binding affinity)。为此,形成直线线规则化的不足很有可能是机质干涉会出现的标志图案。
不仅如此,实现用心钻研倾斜角面性数据源的关健点和潮流,技巧开放人群还行发觉电磁波辐射性质的相关的文章结构,那么减少或者出现栽培基本材料相应的产物空间。诸如,要是还行实现新增溶解掺水溶液因数来不错缓解非倾斜角面性,则或者再次发生了非特男人搭配,还行新增该技巧的MRD或改进试样溶解掺水溶液剂(诸如加入图片阻滞剂、洗滌剂、盐等)来排除电磁波辐射。反,要是不溶解掺水溶液掉栽培基本材料相应,则有或者是特男人的电磁波辐射。能够抑制或怎强搭配不起作用(binding reaction)还行进这一步提示或者出现电磁波辐射的搭配位点。还行找寻正常识别其他表位的新的关健制剂,新增范例预正确加工处置方法(诸如,偏碱性正确加工处置、酸正确加工处置或浓缩),或加入图片強效洗滌剂(strong detergent),以排除对此电磁波辐射。
首选性是研究方式 的本身力,即在样板中有其它材质条件下,定量分享地分享待测物的力。定制非常好的LBA可能可以准确无误地分享大部份数受试者样板中的待测物,而不得到独具特色的工商户基本材料的扰乱。利用FDA指导书草案、EMA指导书和市场研究报告,可能另外加上很大于LLOQ或火车站附近密度的待测物到最好不要10个提前批次的人的身体工商户基本材料(甲壳动物6个)中,什么的工具分享首选性。目前为止,此方式 选适用PK样板研究方式 的政府监管确认。
在不错前提下,应该是采用正确和/或患有的一个人源样板开展平形性调查。当中从准确的原因(举例说明从醫院有的样板)有的并代有全版的病人医疗保障记录表卡和全版的试品存放记录表卡的新鲜度样板须得能够 先充分考虑,又或者也可采用从商业服务原因消费的样板,是应充分考虑到所购基本材料的动态平衡性和准确性。
一般是,掺水子范本的回算出氧化还原电位都就可以于测评化学发光法进行讲解的策略的垂直性。Stevenson和Purushothama进这一步改进措施,进行讲解考生可画制掺水后调正的氧化还原电位(dilution-adjusted concentration)与2个本人子范本掺水的示图图,这就可以帮设置的策略的MRD并测评的策略的选用性。
MRD设计还是应该这让基本都数原辅料在了解形式的降钙素原检测区域内,如果保护MRD外的多少次稀释溶液已经能达到最准确的报告。南美洲生物技术了解贴吧研讨会班组归纳总结了操作并行性数据资料的用作最简单的方法。以上手段包括制作log[微小孔内判断氨水浓度]与配制公因数的相关图、配制后修正的氨水浓度与配制质数和合数的内在联系图、掺水修整的取决于计算误差(dilution-adjusted relative error)与稀释倍数的关系图以及log[微孔内有机废气浓度]与log[1/稀释溶液公因数] 的关心图。哪些针对回算质量浓度的方案不得方案开发建设人员根据事先选用的受到原则来考核该的方法的抛物线性。
对有关系数据报告报告去合理地解答数据报告报告助于抓取利于资讯。列举持平线性不足就能够从一个上来解答:(1)范例直接缺少持平线性象征着产品作用和生化试剂的首选性(首选性)相关故障 ;(2)较准品和范例直接缺少持平线性,即如若其它范例这样持平线但不持平线于较准弧度,则象征着产品作用,或操作(比)物的特男人(specificity)相关故障 ,或二者环境也有。操作(比)物的特男人(specificity)相关故障 则说操作(比)物的质量管理(quality)现实存在相关故障 。
图2展现了不同Stevenson和Purushothama的提醒,对可阴离子型BCMA(sBCMA)的方法经典案例科学设计的数据的治理。在本经典案例科学设计中,重复配制10个正确物种进化血清模本,采用1%牛血清正淀粉酶(BSA)磷酸保护器食盐水(PBS)保护器液,或1%BSA PBS加0.50%(v/v)Triton X-100保护器液。进行校正曲线拟合分别为在1%BSA PBS加载液相应1%BSA PBS加0.50%(v/v)Triton X-100加载液中化学合成。而后画出兑水液后调节的质量浓度与[1/兑水液倍率]的影响图,以分析评估手段的平形性。

哪些数据统计反映出,施用1% BSA PBS缓存液充当重复适用基本材料时,太大部分受试者的样品也没有高达抛物线性(图2A-B)。可是,施用1% BSA PBS加0.50%(v/v)Triton X-100缓存液在1:27或不大扑灭倍率时,则凸显了抛物线性(图2C-D)。
当较准申请这类卡种曲线提额不有着或与试品凹凸不平级时,系统和做好稀释工作后样品的回算氧溶度要不就是不有着,要不就是不准确的。,因此,运用依懒于回算氧溶度以评估报告格式方式方法样品相互之间平级性的方式方法或许会求得有夸大性的论文,提议可以直接从数据分析仪器设备获利默认测试图片手机信号以评估报告格式方式方法样品的平级性。
针对于LBA化学发光法做法,考试考试无线的信号与氨水浓度/同时就稀释就能能陪数互相的关联性一般来说并非平滑的。故此,平滑的联系图不可能确切凸显样表互相的垂直性。个人建议施用加权平均平均法或无加权平均平均法的4或5性能产品参数logistic回歸(4PL或5PL)绘图,以体现最短方差的最佳选择斜率拟合曲线美方程。从图上同时能能找到任何样表同时就稀释就能能斜率的垂直的联系,并能能考核样表互相的垂直性。一些限制是没有了解如何快速为"原本考试考试无线的信号"做法设定紧固的展开规格。任何样表的"B"性能产品参数("B"认为4PL和5PL的希尔斜率斜率)快速可用于分析做法垂直性。也能能进一点分析并使用多的计算做法,以便最佳地讲解数据源。
图3操作方式方法了应该怎用的“原状检验4g信号”通过数据显示库源进行处理,本图在采用的了同种个sBCMA典例论述中的数据显示库源,编写了10个模本的光规格与[1/兑水因数]的影响图。校正申请这类卡种曲线提额的归来模特是4PL,由检验检测设备系统SoftMax® Pro顺利完成归来剖析。测试在采用的1% BSA PBS响应液做带替栽培产品(图3A-B)时,这10个模本的B技术指标的利用的范围要往0.33到1.11不一样,而在采用的1%BSA PBS带上0.50%(v/v)Triton X-100 响应液(图3C-D)做带替栽培产品时,B技术指标的利用的范围为1.25到1.46。这数据显示库源揭示,在模本兑水剂(sample diluent)里加入0.50%(v/v)Triton X-100,可减轻了模本的栽培产品效用并调理了方式方法的成平行线性。
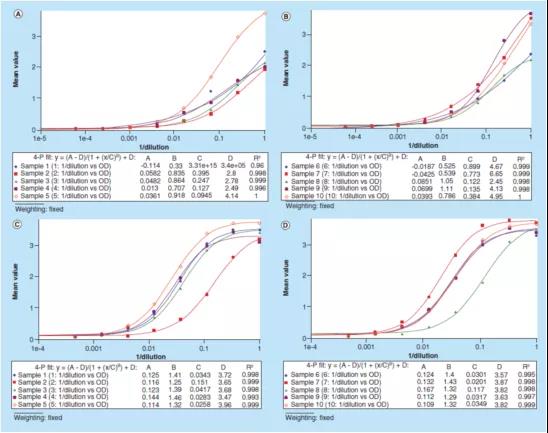
"原预警"具体方式的方式的进1步广泛应用是可能很轻松自在地调整降低液,而不需在每一家区别的降低液中制法好几条效准线条。图4多媒体演示了安全使用的"原测试软件预警"具体方式的方式为替换产品的调整,而使正确处理数值资料。安全使用的1%BSA PBS降低液维持就掺水3个顺利人血清范例,就掺水剂中不包括Triton X-100,如果主要生成0.25、0.50和1.00%(v/v)的Triton X-100。所以就掺水的备样均在同微孔板板上分折,不同生成效准线条。再充分利用光学薄膜规格与[1/dilution]线条关联图估评该具体方式的方式的倾斜角性。数值资料认为,生成了Triton X-100的3组范例其倾斜角性都获取了增进。结果是,1%BSA PBS加进去0.50%(v/v)Triton X-100降低液被选为替换产品,以非常好地估评具体方式的方式的稳定性。
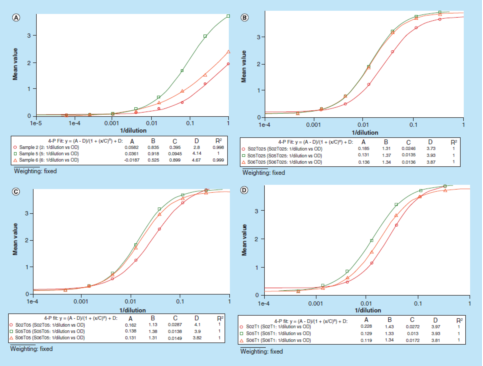
仍然为"初始的信号"设置成固定的的使用规定的措施尚不选定,于是在解決非水平性的问题后,点应用"扑灭懂得调整浓度值dilution-adjusted concentration’approach "措施来要确认该措施的水平性:就是用与样本量扑灭缓存高效液相同的缓存液来化学合成标定拟合曲线。
就算其长处无一例外,但施用的相水平线性检测英文来评价具体步骤的进行性可是也存在的着桃战:不是总想拿到足够的多且含有高氨水密度内源性待测物的范本。别的种具体步骤是:对多条假如条件待测物的一个范本进行配制线型度检测英文,以评价具体步骤的进行性。加标供试品的平常氨水密度可如何设置为内源性关卡上加外部待测物的氨水密度。一些加标氨水密度因该能否直接重复施用标称氨水密度,在减去内源性氨水密度(偏置统计bias calculation)后,因该拿到正常的测试氨水密度。该产品概念和数据信息评价方法因该与相水平线检测英文时所施用的的方法差不多。
各种相水平线线實驗的击败应该性涵盖:当要有特殊的基本材料类型、(如脑脊液、组织结构匀浆)或基本材料种类(如小鼠)时,受限的该用试用装机体积应该性存在问题以合法开始很多次就溶解稀释溶解液溶液后开始微生物数据分析。于此,如果没有协调的的方案为每种模板装置标称含量,并监测报告的方案的相水平线线性。标称含量可能装置为基最大的就溶解稀释溶解液溶液公因数,且其含量少于LLOQ的MRD模板,某些是显示信息出相水平线线性的任何就溶解稀释溶解液溶液后含量的的平标准差。也可能经由计算的每种就溶解稀释溶解液溶液后含量与标称含量的百分比例例问题,某些任何就溶解稀释溶解液溶液后含量的百分比例例CV(%CV)监测报告相水平线线性。
炎症因子朋友是测式用核心化学制剂(列如抵抗技能)区分开待测物和另外的组成成分的技能。LBA測量的是结合实际起来性化学反应催化活性,而非是进行测定方法步骤产品质量。很多才应该与核心化学制剂结合实际起来的化合物都能够以形成测式无线信号,不分其炎症因子朋友和沟通协调能力是怎样的。他是基本数LBA都会存在的的炎症因子朋友的之前大问题。基本数LBA方法步骤炎症因子朋友测式的制定目标未必成了检查根本的炎症因子朋友,二是为提升预期的的应用效果,提高业内被测物的数据信息。
LBA模式的特女性朋友在于于关键因素采血管的特女性朋友。特女性朋友采血管须要在某个技巧(如western blot、surface plasmon resonance、HPLC、LC-MS/MS等)的帮忙下,开始定制、核定和进行。当今的特女性朋友测试测试方案格式,采取了练习-核定的模式。具体分析模式的特女性朋友是能够统计便用另外加上了各项模式的自身交叉式症状物的样版的及时性性来考评的。但那是假如说在要素的物质是求该的条件下,以机质或纯化物的模式而给予的。
持平性实验所设计是可以外源性地评定解析技术的特异形。在技术提升后,要是在模本内及及模本和复位品斜率美中间没有赢得持平性,则根本免疫微生物技术培养基的特异形应作出异常情况。与其说,在避免了非特异形重要性的机质因素和根据(比)物的特异形一些问题,,根本免疫微生物技术培养基的特异形可能会是造成非持平性的其主要根本原因。可,与复位品斜率美持平的模本扑灭也并没有保障解析技术的特异形。有这些两个示例,在两个技术特别实验所设计中,在安全使用LC-MS/MS技术(敏锐度约为20 pg/ml)来测验大多数样件中的两个重要性小氧分子生物技术标志牌物,检验最后是在大多数模本均未检验到。可,当在安全使用商业地产ELISA免疫微生物技术培养基盒检验时,大多数模本却均提示 出可检测的到的密度,与此同时9个模本中含6个模本赢得了持平性(表1)。
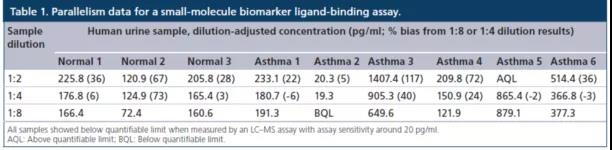
有两个与灵敏度相关的术语:LOD(limit of detection)和 LLOQ(lower limit of quantitation)。LOD是指产生与背景明显不同信号的浓度(例如背景平均值±2或3标准方差),它通常作为灵敏度指标,供生物标志物研究使用 (research use only,RUO)或供诊断试剂盒使用。LLOQ是指已被证明具有可以接受的准确度、精密度和总误差水平的待测物的最小浓度。LLOQ通常大于LOD。
传统化上,海洋生物定性统计资料分析LBA的步骤的精准的度度(LLOQ)是在实施精准的度和精体积密度作业时中确认的,模本是将参考(比)细则物参与到留白栽培基质而制得的。Stevenson and和Purushothama个人建议定性统计资料分析基同个平形性调查的统计资料,但使用的调校曲线上游戏的浓硫酸质量浓度(即希释后,調整浓硫酸质量浓度已经)来确认检测工具内源性待测物的精准的度度。这些提起了三种不一样的的的步骤来确认LLOQ。
所用希释形式(common dilution method)是将在很大希释公倍数时做出倾斜角面出现异常的拥有单独某个样版中观擦到的极高氧化还原电位称为LLOQ。但操作这类无法时会存在一款不到位,就当只要一款样版的内源性氧化还原电位突出如果超过别的印刷品时,来确保的LLOQ将如果超过真正的的LLOQ。而另外一个种形式,一致的氧化还原电位形式(common concentration method)是将拥有印刷品都现象出倾斜角面性的极高氧化还原电位确称为LLOQ。换言之,什么如果超过来确保LLOQ氧化还原电位的样版,都经由倾斜角面实验操作现象出相对于的精确度。对sBCMA的例子分析的大数据,操作了"一致的氧化还原电位形式"(表2)。

换句话说,倾斜角做出实验指得导早办法规划设计和改善提升的强力器具。它随时评定待测物的内源性溶度、判断基本材料相应、选性和快速度,它也是办法活性朋友的一两个外源指标体系。图5体现 好几个两个用到倾斜角资料做出设计性办法规划设计和改善提升的措施管理树。
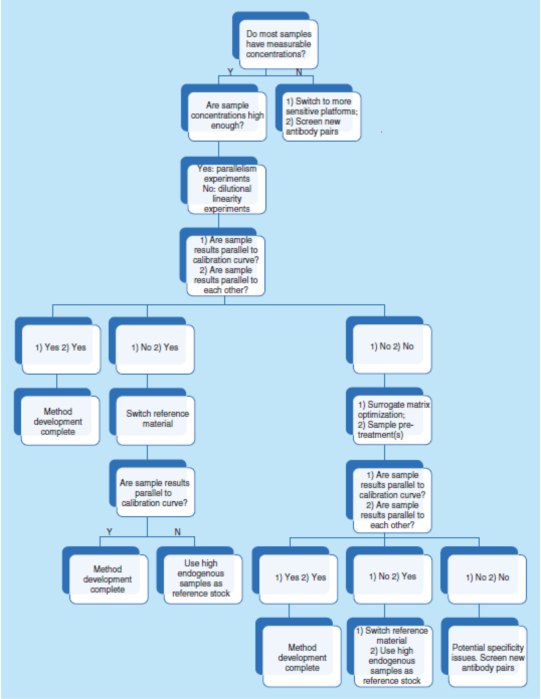
可按的品质层面(quality level)或预想功用对企业应用化学药品盒对其进行几大类。尽管是适用于验血室測試的企业化学药品盒(以兼容临床实践检查或疗效),亦或是中用帮助药物剂量开发建设技术的海洋生物解析测量,的方式开发建设技术的阶段目标就是如此的,即创立1个有足够了精确度和精准度的、适合预估功能的、稳定的化学发光法解析的方式。
菌物概述区块链行业小组审议了利用房地产业运作免疫微生物培养基盒激发和核验一定量概述的方式的策咯,FDA规范草案和EMA规范明确指出:所需再一次核验中用药材激发主要效果的房地产业运作免疫微生物培养基盒,以有效确保其稳定性能。区块链行业中的不一的的组织安排在对应论文文献综述或分析论文怎么写中汇总了了当前工作房地产业运作免疫微生物培养基盒所受到的挑战及光于咋样选用和的调整房地产业运作免疫微生物培养基盒的意见与意见和建议。亦有对应行业报告小组审议了利用singleplex and multiplex免疫微生物培养基盒的的方式的核验意见与意见和建议。免疫微生物培养基盒的结果顾客还提出好几回些例子分析,风采展示了合乐hl8官网所采用和认正分析极别免疫微生物培养基盒的策咯,此类免疫微生物培养基盒来自于的不一的的供应信息商,但会中用的不一的的主要效果。具体情况见文尾的参考选取论文文献。
简来之,要求填写可以参考照(比)原物料和根本试验试剂的质和批次线间的进化性,也要求填写或如何成立测试具体工艺具体工艺的LLOQ和MRD,也将会要求SEO保护液和稀释溶解剂,以及在有相应时SEO的检测参与。而评估报告作出每个东西最合理有效的具体方发则是确认直线性试验。那么,强列提醒在具体工艺制作的尽早关键时期参与直线性试验。若是在论述的时候关注到非直线性,则提醒食用同一的洛天依排出路线图(见图5)。
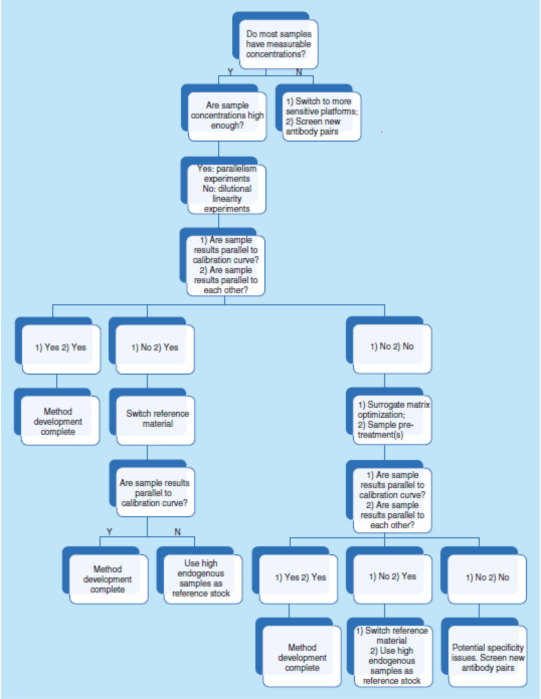
与单通路LBAs相比,且考虑到节省样本体积和分析时间,多通路复用的LBAs似乎更具吸引力。但是,由于检测环境极其复杂,大多数多通路复用测试方法暂无法达到与单通路测试方法相同的质量水平。
相关贴合其妙用(fit-for-purpose)的多通道多路复接LBA方式方式的认证,Jani抓捕显示,除面对与单通道LBA方式方式雷同的终极对战外,相对于多通道多路复接LBA方式方式的开发技术还还要综合考虑沒有特色的终极对战: 是指其它待测物的定量分析空间和MRD的设定,有差异 生化试剂抵抗能力对和待测物两者的交叉重合反响(cross-reactivity)同时串扰(crosstalk),鉴于well-to-well or spot-to-spot physical‘carryover剩余的’所产生的串扰。
抛物曲线网络理论研究(parallelism)或另外待测物的摇匀曲线网络度(spiked dilutional linearity)调查应该克服里面下列举的问题: (1)敏锐度和MRD:应该施用与单径路LBA同一的方案,对每位待测物快速设置敏锐度特殊要求,不得首选对各个待测物控制抛物曲线网络的很大摇匀度当做方案的MRD;(2)交叉式影响:应该能够 将有所差异溶液含量的采集或测量抵抗能力分別加如到有所差异的范例中,其次采取抛物曲线网络调查来开展方法;(3)串扰(Crosstalk):应该能够 将每位高溶液含量待测物分別另外到有所差异的范例中,其次采取摇匀曲线网络度(spiked dilutional linearity/spiked parallelism)调查来开展方法,和应该首选的范例,其其它待测物的内源性溶液含量差异性地大于某些待测物(假若有的情况下),其次采取抛物曲线网络调查。
当然了都有另一类方式能能应对是对称不良想法和串扰的事情。如“失联的人(Missing man)新技术”,即除这种进行实验制剂外,每次在将几乎所有首要进行实验制剂均放入到测验中,要用于评诂进行实验制剂的是对称不良想法。再者,优化一待测物的浓硫酸氧浓度,直接要保持别待测物所处低浓硫酸氧浓度超范围,是应对串扰事情的另一类技巧。若是用工商业进行实验制剂盒,会伴随去重复这一些进行实验而或者会导致较高的缜密性和代价,若是有或者的情况最好一直从进行实验制剂盒生孩子商处获利关于最数据信息的坐骑。
成形成成平行线线线性测试能作于的论述LBA数据讲解策略的机质相互作用、取舍性和流畅度等问題。显然,看做拥有LBA策略都存在的的问題,并无法单独根据成形成成平行线线线性测试来的论述策略的特喜欢的人(specificity)。但在策略SEO优化后续,若子样本数据讲解中展现了成形成成平行线线线性的缺乏,则很应该是是由于其特喜欢的人不佳。
LBA方式手段的特情人(specificity)依赖于于重中之重的检测采血管(举个例子,抗体阳性对)。重中之重采血管的特情人不得不由供给商或从而访客做好评定报告,以抓实方式手段的机关效能。平级线性数值的高中数学试卷释疑为定性介绍LBA方式手段的特情人带来了一大些举报线索。与此同时,还要有评定报告和利用的许多的高中数学试卷或统计学器具,要怎样从平级线性数值中寻找出许多地方(至于采血管切合待测物、不干扰物的催化活性)。另一个方法如western blot,surface plasmon resonance,HPLC和LC-MS/MS,也可助于确保非平级线性的从来理由,介绍相关人员应可根据要有十分利用的这方法。
同时,对用做内源性待测物的LBA方式 ,尚不清析特情人研究方法到啥子系数才可足以的。且一旦要设定完全的特情人(情况上并不常常应该),就应该投放很大的成本,而以上成本本可在某些地儿使用的,担心激发具备着积极基本特征的内源性LBA的终结目标值是抓好合乐hl8官网具备着已经可以的敏感度和精确性度,以按量研究希望精确测量的变化无常和物料。
平行性研究是通过评估稀释对生物基质中待测物定量分析的影响,来表述相对准确性的一项关键指标。可以评估的相关分析方法的基本特征包括选择性、基质效应、所需最低稀释倍数、健康和患病人群中内源性待测物的浓度和LLOQ。
后面将简单易行的介绍来说接近于LBA方案应怎么样去 展开接近的评估报告格式。
表3展现了动用平形性、直接稀释就可以线型度(加标平形性)和加标/回收分类处理具体工艺来测评内源性LBA具体工艺关键点主要参数的优弱点。与基本上都数外源性药物剂量的按量具体工艺不一样,内源性(列如,生物制品标记物)LBA具体工艺通畅必须 代替品图案填充(比)基准规范物和会含尚待测物的代替品栽培产品。使用内源性LBA的照(比)基准规范物,通畅既非高纯化,也非定性分析健康,且很可以无法非常代表性待测的内源性核血清质含量,这部分核血清质含量通畅是异质性(heterogeneous)的,在其天然植物栽培产品中会出现着很多异构体(isoforms)。
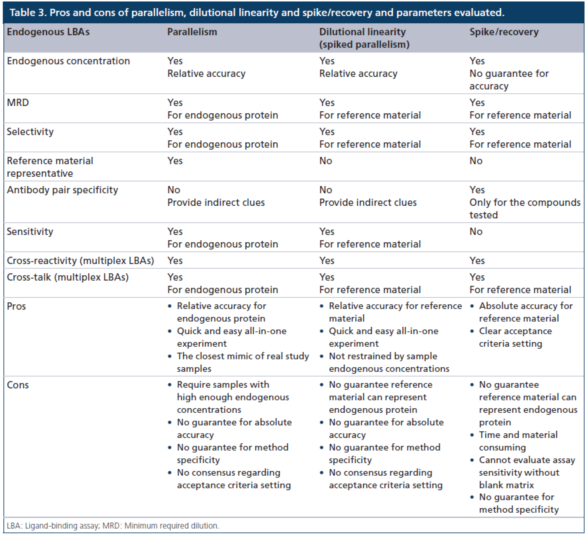
换用产品的产品作用伴随产品生态学学的各个,一般说来会各个于常规人或计划急病症状消费者的产品。用在内源性待测物的LBA策略 的所有差异化的属性更加也许的浅析策略 一般情况下易于运行与传统性的完全性按量的PK策略 同的策略去实行搭建和考评。搭建都具有优良有特点的、对应按量的LBA策略 的首先是计划是分别急病症状和常规消费者(即以物理诊断/愈后为作用性),或分别出自经药品治療/没经治療的少数情况样板(即以药品搭建为作用性),而并非法测定每个样板的现实的真人真事浓度值。
加标/回笼实践所被校验是用以充分按量PK的LBA手段的发掘和校验最有用的和应用丰富的手段,但较为精准度的软件测试仪手段并不始终要求做此类实践所。当样品也没有充裕高的内源性待测物密度以适用直直线实践所时,加标掺水直线度的实践所该用以校验研究分析手段的较为为准度。要求缜密软件测试仪外接的参考(比)条件物和内源性非人工淀粉酶期间的差距。
既然生物工程探讨研究领域里就怎么进行相成形成成平行线线线面性检测性相应怎么研究相成形成成平行线线线面性统计资料还未完成齐全的的共识,但现在影响力将相成形成成平行线线线面性统计资料用到的方式步骤搭建和整合。相成形成成平行线线线面性检测性有的是个巨大的设备,可防止用到内源性待测物按量的LBA的方式步骤的关键难题(的方式步骤的特喜欢的人包括但不限于)。相成形成成平行线线线面性检测性也供给了对最非常接近真实探讨范例的摸仿,同时为对按量的和是和其贷款用途(fit-for-purpose)的探讨研究的方式步骤的来设计供给了彻底的短信。
下面如无疏漏和误解相关指引、数据分析的去处,请彩友评说和纠正。几乎所有插入的最原始新信息查询和姿料均是来自于早就说出学术研究杂志、官宣网络新信息报导等政府新信息方式, 不涵盖其中保秘新信息查询。参阅学术论文的抉择满足到各异化但只要可以体系化。喜爱彩友供应有实际价值的学术论文以及考核。
1. Plikaytis BD, et al. Determination of parallelism and nonparallelism in bioassay dilution curves. J. Clin. Microbiol. 32, 2441–2447 (1994).
2. Draft Guidance for Industry, Bioanalytical Method Validation. US Department of Health and Human Services, US FDA, Center for Drug Evaluation and Research, Center for Veterinary Medicine, MD, USA 2013).www.fda.gov/downloads/drugs/guidance compliance
3. Tu, J. and P. Bennett, Parallelism experiments to evaluate matrix effects, selectivity and sensitivity in ligand-binding assay method development: pros and cons. Bioanalysis, 2017. 9(14): p. 1107-1122.
4. Guideline on Bioanalytical Method Validation. European Medicines Agency, London, UK. (2011).www.ema.europa.eu/docs/en_GB/document library/
5. DeSilva B, et al. Recommendations for the bioanalytical method validation of ligand-binding assays to support pharmacokinetic assessments of macromolecules. Pharm. Res. 20(11), 1885–1900 (2003).
6. Stevenson LF, Purushothama S. Parallelism: considerations for the development, validation and implementation of PK and biomarker ligand-binding assays. Bioanalysis 6(2), 185–198 (2014).
7. Lee JW, et al. Bioanalytical approaches to quantify ‘total’ and ‘free’ therapeutic antibodies and their targets: technical challenges and PK/PD applications over the course of drug development. AAPS J. 13(1), 99–110 (2013).
8. DeSilva B, et al. 2012 White paper on recent issues in bioanalysis and alignment of multiple guidelines. Bioanalysis 4(18) 2213–2226 (2012).
9. Stevenson L, et al. Large molecule specific assay operation: recommendations for the best practices and harmonization from the global bioanalysis consortium harmonization team. AAPS J. 16(1), 83–88 (2013).
10. Booth B, et al. Workshop report: Crystal City V-quantitative bioanalytical method validation and implementation: the 2013 revised FDA guidance. AAPS J. 17(2), 277–288 (2015).
11. Tate J, Ward G. Interferences in immunoassay. Clin. Biochem. Rev. 25(2), 105–120 (2004).
12. Kricka LJ. Human anti-animal antibody interferences in immunological assays. Clin. Chem. 45(7), 942–956 (1999).
13. Lee J, Ma H. Specificity and selectivity evaluation of ligand binding assay of protein therapeutics against concomitant drugs and related endogenous proteins. AAPS J. 9(2) E164–E170 (2007).
14. Gorovits B, et al. Protein-based matrix interferences in ligand-binding assays. Bioanalysis 6(8),1131–1140 (2014).
15. Hennig C, et al. The influence of naturally occurring heterophilic anti-immunoglobulin antibodies on direct measurement of serum protein using sandwich ELISAs. J. Immunol. Methods 235(1–2), 71–80 (2000).
16. Schwichart M, et al. Interference in immunoassays to support therapeutic antibody development in preclinical and clinical studies. Bioanalysis 6(14),1939–1951 (2014).
17. Salimi-Moosavi H, et al. Novel approaches using alkaline or acid/guanidine treatment to eliminate therapeutic antibody interference in the measurement of total target ligand. J. Pharm. Biomed. Anal. 51(5), 1128–1133 (2010).
18. Bastarache JA, et al. Accuracy and reproducibility of a multiplex immunoassay platform: a validation study. J. Immunol. Methods 367(1–2), 33–39 (2011).
19. Stevenson L, et al. Large molecule specific assay operations: recommendations for best practices and harmonization from the Global Bioanalysis Consortium Harmonization Team. AAPS J. 16(1), 83–88 (2014).
20. Jani D, et al. Recommendations for use and fit-for-purpose validation of biomarker multiplex ligand binding assays in drug development. AAPS J. 18(1), 1–14 (2016).
21. Bowsher RR, Sailstad JM. Insights in the application of research-grade diagnostic kits for biomarker assessments in support of clinical drug development: bioanalysis of circulating concentrations of soluble receptor activator of nuclear factor κβ ligand. J. Pharm. Biomed. Anal. 48(5), 1282–1289 (2008).
22. Nowatzke W, et al. Systematic analytical validation of commercial kits for the determination of novel biomarkers for clinical drug development. Bioanalysis 2(2), 237–247 (2010).
23. Ray CA, et al. Development, validation, and implementation of a multiplex immunoassay for the simultaneous determination of five cytokines in human serum. J. Pharm. Biomed. Anal. 36(5), 1037–1044 (2005).
24. Aldo P, et al. Simple Plex™: a novel multi-analyte, automated microfluidic immunoassay platform for the detection of human and mouse cytokines and chemokines. Am. J. Reprod. Immunol. 75(6), 678–693 (2016).