

























跟随中国激厉药物研制开发、otc药品审评审员批机制的重要性改制的快捷推广,化药申请分类整理、市场销售批准持有人人机制的重要性等重磅消息政策性的现已国家,国家药物研制开发是暖春。面对试图在创药物范畴深入的从业人员者来说,怎么样洞察vscode,乘势谓之,或将为在未来成败得失的至关重要。
对此,武汉合乐hl8官网医疗器械微信民众号民众号诚邀微生物体体理论研究分折领域专家、合乐hl8官网医疗器械子大公司山东博瑞副负责人负责人袁智博后,新开设“袁来尽管”研讨专栏,就大原子核微生物体体理论研究分折、药代干劲学等有关的为题拉伸研讨理论研究,盼望经过有关的学识与经验值的安利,造成非常多青年文学的议论交换,下载加速复兴中国有的微生物体体医疗器械产业的经济发展经济发展,拨冗莅临垂注!
这段话为“袁来这些”栏目的最篇,主要是要根据已发稿的参考文献材质,对与大氧分子生态学解析相应的的小知识实施系统化地解绍。
配体通过式检测步骤(LBA,也喻为immunoassays)就是一种选用的分析一下方法,使用在选择与任何动物团伙的相互结合作用(binding interaction),降钙素原检测检验怪物原子核结构(总体要求浅析物,Analyte)在怪弹簧测力计液中的质量浓度。LBA规定每组用其中一个怪物原子核结构来降钙素原检测总体要求浅析物,这样怪物原子核结构一般被誉为关键所在试剂,须都可以特女性朋友地通过方向概述物。
LBA可有两个类:(1)高效液相联系软件测试仪,其工作目标讲解物与标记图片过的判断试仪剂当中的联系反应迟钝有在溶高效液相(图1A);(2)固相联系软件测试仪,另外某个的关键实验化学药品被特定到液体表层,如微小孔板或树脂胶(图1B),以采集样本中的学习对象浅析物。色谱仪试验常常需求分離方法,如色谱或电泳或离心力,所以将学习对象浅析物-标出检试验剂从不结合起来的氧分子中離起来做按量。
在使用上,LBA是首要的考核动物工程药PK/TK时的主要的定量解析解析方式之中,该方式的特女性朋友和确定性依赖于于目标值解析物与一些动物工程团伙(如感觉、重要性得票率动物工程药的抗体阳性和核酸更换体(aptamer))的之间使用。
该方案中可求察到机器设备异常与生物学药的浓度值举例说明关联,或者说,在线检测信号灯的来历是酶化学体现工业体现或蔓延化学体现工业体现,而这类体现则是所有双方融合做用(binding interactions)的有部门。
通常如何理解,大原子的电磁学化学物质特征無法会直接诞生论文检测表现,不许于这样的话的一定量浅析策略。重要理由最为他们binding interactions的核心本质,LBA的标(校)准的身材曲线的新动态(酶联免疫法)范围图会比较梗塞,同一时间也并非规则化,S型的(sigmoidal curve)。
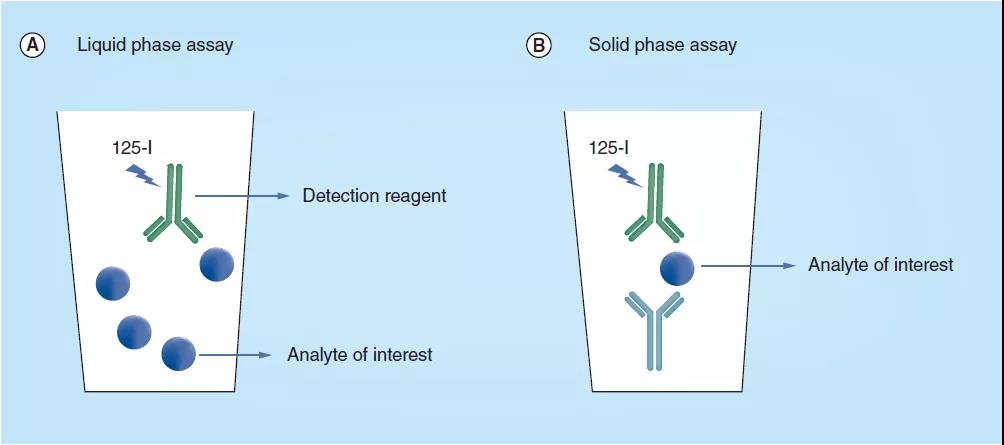
如图是1如图所示,在高效液相测式中,构建现象在液体中发生,至少一些工作制定目标分享物与箭头过的判断化学药品根据,最后再完成前因后果的分割进行将工作制定目标分享物-箭头判断化学药品从来没有根据的原子中分发型割粗来。
在固相测试英文中,一位关键点化学药品被不变到液体表皮,如纳米纤维板或硅橡胶,此化学试剂在粉末状外表综合关键分析一下物,因而造成未综合的原子核被转移出来的。
Yalow和 Benson于1960年开发管理的测得合乐hl8官网人类胰岛素的方式方法,是蔓延免疫细胞测得(RIA)的符号性举例说明,Yalow所以说于197七年换取诺贝尔奖。简单的地说,也是能够用鱼精蛋白锌牛胰岛素或商业地产传统牛胰岛素免疫系统豚鼠,以赚取当作该RIA具体方法重点制剂的胰岛素构建抗原。
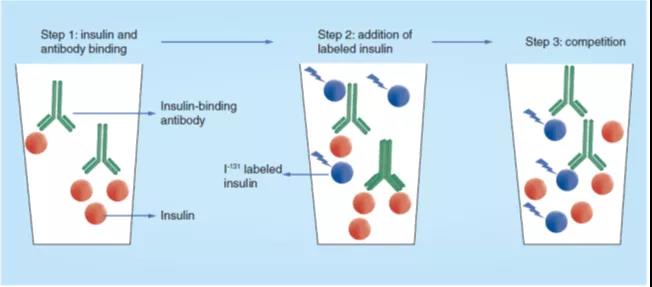
在这的办法中,会因为没有社会胰岛素的成果体,对此I131标注的晶体牛胰岛素(胰岛素-I131)被应用于示踪剂。此 RIA 的方式是针对范本中的人胰岛素与豚鼠血清中的胰岛素配合抵抗能力的大力配合(图2中的步奏1),并让已知a氧化还原电位的胰岛素-I131与该免疫抗体的紧密联系竞争力(图2部骤2-3)。胰岛素-I131与胰岛素配合免疫抗体的配合在液体中去,矿酸的胰岛素-I131与配合了抗体阳性的胰岛素-I131的脱离确保纸色谱电泳技木确保,这就能让按量测定法胰岛素-I131被选为概率,其象征了样版中胰岛素的氧化还原电位。这里手段中,评均可按量的胰岛素氧化还原电位为1.4μU。
在这一个有计程表碑寓意的调查发表论文,,RIA在20个世际前中期能够能够了宽泛的软件。在用到适度的具体制剂时,RIA迅敏度和采用性都良好,其知具体考验包含用到和治理放射学线性食材的同意证规定、放射学线性放射性核素的图标错误率、利润以及有效的半衰期。在RIA能够能够软件的十二年内,即20个世际的7080年代初,就出现了了非放射性核素免疫性力检测判断,如酶免疫性力检测判断(enzyme immunoassays,EIA),EIA一般说来被成为ELISA,即酶联免疫性力检测溶解耐压(enzyme linked immunosorbent assay)。
Engvall和Perlmann在197半年内容中第一次描术一堆个降钙素原检测兔抗体球蛋白质G(兔IgG)的ELISA形式。其原因都是从羊血清中去除的抗兔IgG应用于综合荷兰猪IgG,行而综合了了种酸碱度磷酸酶(ALP)的兔IgG被能够满足与兔IgG主动恶性竞争和抗兔IgG血清的综合,与此保持含量与检测设备设备崩溃(无线网络信号)内的原因,转换成的检测设备设备无线网络信号与范例中的IgG量相差悬殊。如今技术性的不停的经济发展,知识界相结合了有所不同的酶,如辣根过非金属氧化物物酶(HRP)、β-半乳糖苷酶(GAL)和荧光素酶(luciferase),不使EIA拥有与RIA很的精准度。

图 2. Yalow这一发觉的胰岛素牵扯免役测试的道理图。样板中的胰岛素在悬浊液中与抗胰岛素血清紧密结合(布骤1),再把已发现氧化还原电位的I131标识的牛胰岛素加到反映悬浊液中(布骤2),样板中的胰岛素与I131标识的牛胰岛素(布骤3)双方竞争者与抵抗能力的通过。适用人胰岛素配制的标准规范身材曲线和胰岛素抵抗能力通过的I131符号牛胰岛素的氧化还原电位还可以统计模板中被置換的胰岛素的渗透压。
激烈式ELISA制式是根据初始状态的胰岛素RIA和IgG EIA最简单的方法中的通过激烈。产于样本的最终目标分享物(analyte)和对比分享物(reference analyte)与数据分析物活性朋友的抗体阳性紧密联系当中的的竞争是这种格试的关键因素。
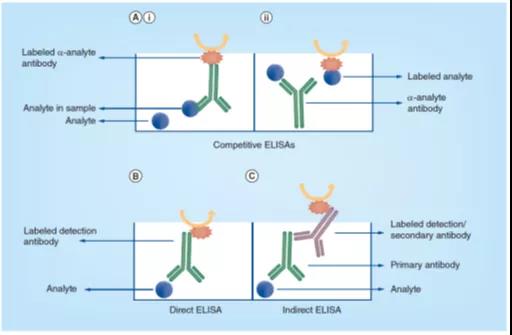
抵抗能力或要求进行分折物都能够 以标识酶,食用于构建的发应。食用标识抵抗能力(图3Ai)时,根据进行分折物第一方面坐以地溶解到砂芯过滤器板的孔中,第三参与有要求进行分折物的样例,如生殖细胞裂解液、血清等,并与不变溶度的标识抵抗能力来孵育。样例中的要求进行分折物与不变的进行分折物寡头垄断,以构建受限总量的标识抵抗能力,接着随后的酶的发应导致的走势与样例中要求进行分折物的溶度成正比。或许,能够 食用固相溶解的抵抗能力和标识进行分折物(图3Aii),样例中的要求进行分折物与不变总量的标识进行分折物统一孵育,并与之互相寡头垄断和不变抵抗能力的构建。与上的实例中一个,产生的走势与样例中要求进行分折物的溶度成正比。
间接性式ELISA是最简易的ELISA文件后缀,试品中的计划深入研究分析物物理吸附到细孔板的孔中,利用酶偶联生化试剂或图标测试表面抗原,间接性保证 计划深入研究分析物的测试,如图已知3B如下图所示。
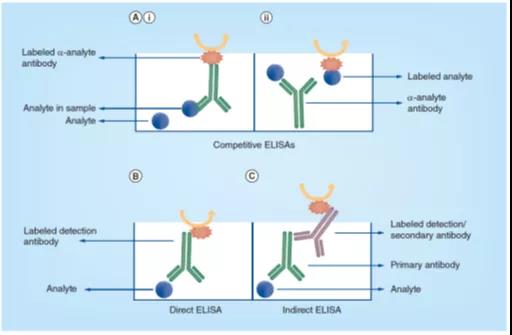
图3. 竞争力式(Ai & Aii)、会(B)和间接性(C)ELISA测试测试形式的方式图。关键阐述物(Analyte)表示被测定方法的关键球膳食纤维。在角逐式ELISA中,是可以箭头关键阐述物或抵抗能力,而在直观或间接性ELISA文件格式中,只箭头检验抵抗能力。
间接ELISA类似于直接ELISA,两者间主要差别在于主要(primary)抗体未被标记。目标分析物的检测是通过再次添加一个酶偶联试剂或标记检测抗体,使其与主要抗体结合而实现的,如图3C 所示。
之间ELISA更好速,是因为它比外源ELISA少一家工作步骤。它一般性适用所需更快的完全的常见检查,商业楼化的家装怀孕前检查那就是那样版式的一家例子。而相互性ELISA尽管较立即ELISA多这个方法步骤,但手机信号变大基本强于立即ELISA。因,相互性ELISA基本比立即ELISA更神经敏感,就能够预估更低丰度的蛋白酶质。
正如同图3C 表达,外源ELISA较一直ELISA上升的关键步骤就是原于于样表的计划解析物一直物理吸附到细孔板,但愿意达到这种的治疗效果,亦有特定的等级。因在洗板操作步骤中,几率会洗掉关键数据分析一下物,这样几率会增多測試的遗传变异形。除此以外,非特异形地组合到纳米纤维板的以外的别的蛋白质几率影响假阳型可是。因为应对上面的考验,以外的别的耐用性会高的形式因此具象化下来,这当中有通畅被是指夹心、桥联或相互竞争性ELISA(在夹心或桥联ELISA形式中),在此类形式中,一类能与关键数据分析一下物特异形组合的生物工程免疫试剂前提是被气体吸附到纳米纤维板中。
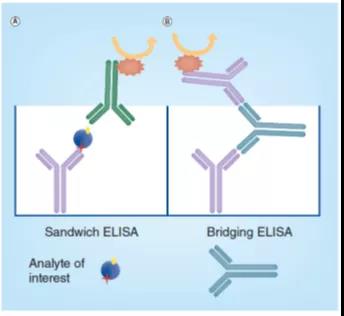
图4. 夹心式ELISA(A)和桥接式(B)ELISA的设计原理图
夹心式ELISA需求两位差异的实验制剂或抗体阳性,的主要用来阻止,另的主要用来探测工具的任务研究介绍物。哪些实验制剂与的任务研究介绍物的差异表位(epitopes,联系实际位点)联系实际,而使确立夹心式制式(图4A),对此会产生的之间的作用存在特意高的特喜欢的人(担心阻止和探测工具进行都需求特异的表位识别系统,这样才能制成探测工具讯号)。
桥联ELISA较常用于测定方法更具好几个一样的抗原依照位点(2价)的抵抗能力或其他的工作目标研究物的密度,也可以标识与阻止同等的微生物培养基,用做在线检测一些二价的任务研究分析一下物,故此,要求研究分析一下物可被算作采集和检验化学制剂中的桥梁结构(图 4B)。夹心或桥接ELISA 格式均可设计成为竞争式的ELISA。
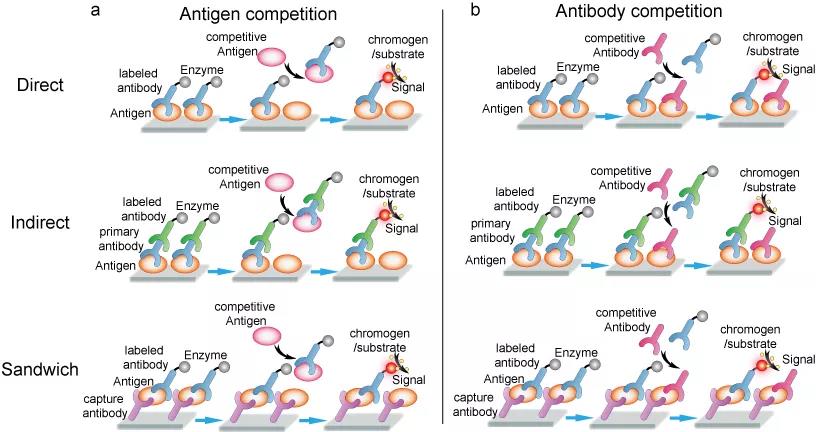
以上所述模式是ELISA的几乎设计,一切模式也就就可以以选择良性相互竞争力或限制需求用以优化,来测量抗原或表面抗原(图5),一切措施都需求与微生物培养基二次想法/孵育才就可以提升最适宜情形。哪些最适宜情形就就可以经过加抗原(图5a)或表面抗原(图5b)来享受对决。时间推移溶剂中下游离的抗原(表面抗原)的增多,要与进行固定底物(immobilized substrate)组合的表面抗原(抗原)的数目则减低。洗滌方法后,加生色剂底物(chromophore substrate)以产生了数字无线信号(颜色搭配變化无常或变色)。表面抗原/抗原对决产生的数字无线信号變化无常表明了管于良性相互竞争力性抗原/表面抗原的讯息。良性相互竞争力式ELISA针对测量很复杂混合型物中的抗原氨水浓度比较有用吗,非常是在也许内含抗原的异常产品的样板与内含已知a数目的纯化抗原的累似产品的样板时。
天然免役表位(epitope)是快穿之女主天然免役软件寻常可以判断的抗原氧分子的一本分。当抗原的表位以非共价键的的方式两者之间所引导制造的抗原肯定定互补式性的区域划分(complementarity determining region)上下级能力时,也会遭受特情人的判断。
免疫表面抗原吸引力(affinity)说明免疫表面抗原与此单个指标值了解物(analyte)/抗原(antigen)联系的烈度(intensity)或比强度(strength),由解离常数(Kd)指代。低吸引力免疫表面抗原与抗原联系弱,加容易解离;而高吸引力免疫表面抗原与抗原联系如此强,在屡次的洗洁步骤之一中不可解离。从ELISA的多角度看看,再者是第一选择,常见用以猎取指标值了解物。
亲和度(Avidity)是测定的抵抗能力与很多个抗原确定成分(antigenic determinants)融合的一体化刚度的招生指标。抵抗能力对某的融合位点的责任心并不总能呈现抵抗能力-抗原双方意义的刚度,随后抗体球蛋清G(IgG)有好几个抗原紧密紧密运用位点(2价),而IgM有10个抗原紧密紧密运用位点(10价),亲和度说道IgG或IgM的,各用这对二个或10个抗原碳原子的纵向紧密紧密运用难度(overall strength)。
重要的制剂
的ELISA技巧偏重要的包含位置是测式微海洋生物体技术学培养基,它取决于了ELISA技巧的流畅度、特异形和技巧的水平。ELISAs较为常用于用药发掘:在PK测评中,一定量测定法法血清海洋生物体技术学药的溶度;测定法法内源性血清和海洋生物体技术学标制物;验测抗用药表面抗原的存在的以做出免疫检测力性原性测评等。LBA技巧最好的关键因素微海洋生物体技术学培养基是单克隆表面抗原(MAbs)或多克隆表面抗原(PAbs),而不算重新组合靶标血清。考虑到生产PAbs或MAbs,还要将海洋生物体技术学药或海洋生物体技术学标制物血清极其佐剂或的载体,依据涉及应用给到应该的寄主细胞小动物外来外来物种上做出免疫检测力性。对待PAbs,小兔子、小羊和山羊是最较为常用的寄主细胞外来外来物种,所以二者的体重大(生产的表面抗原量也大),更易找出动静脉和健壮的免疫检测力性想法。
用来免疫细胞的各个方面个抗原都极高更复杂的,担心它都可以显示大量的,能被差异的淋疤生殖細胞辨识的表位,这一些淋疤生殖細胞那么被刺激启动。刺激启动了的淋疤生殖細胞分裂繁殖,生殖受损癌细胞膜分化成浆生殖細胞,并分沁出多克隆抵抗能力阳性的混体。PAb库(混体)是指了差异抵抗能力阳性的汇集了目标群体,这一些抵抗能力阳性能辨识抗原的俩个表位(在使用ELISA浅析)。为了让生产方式MAbs,必须要进那步区分单一淋疤生殖細胞,并与骨髓瘤生殖細胞融为一体,以会产生了不死不灭的杂交种瘤生殖細胞,然后持续时间会产生了指定区域的MAb。以至于,相同个克隆(clone)的抵抗能力阳性只辨识一种抗原的单一表位。在ELISA中会过于频繁地在使用MAbs或PAbs,其取舍(相对 多种不同ELISA各式某种程度)在于于不少来考虑条件:如可及性(Availability)、责任心、特男人(Specificity)和交叉的情况化学反应性(Cross-reactivity)。
免疫抗原的炎症因子朋友(specificity)是炎症因子朋友地组合起来相关抗原的力量,与ELISA方案的决定性(selectivity)尽为差不多,但相关。决定性就是一个酶联免疫法浅析方案,在某些暗藏不干扰部分会有的事情下,从众心理多某些不会改变的淀粉酶质中辨别和酶联免疫法测量的工作制定指标浅析物氧浓度的力量。相交反映性(cross-reactivity)说的是免疫抗原与除的工作制定指标抗原之下的某些多抗原组合起来的力量。当抗原(的工作制定指标浅析物)的与免疫抗原化学化学制剂组合起来的表位与某些淀粉酶质相像时还是会出现相交反映。普遍来,炎症因子朋友和相交反映性对ELISA方案的决定性和基本材料效用有很多损害。如果用到高人格魅力免疫抗原充当截获化学化学制剂,免疫抗原/的工作制定指标浅析物的结合物就都可以在含有多淀粉酶质的“搅拌物”样本有效地生成,基本材料效用会随着降底,而方案的决定性结果会拥有完善。
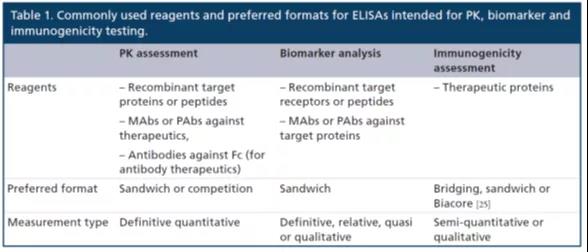
表1总结怎么写了ELISA应该用些的制剂和各种类型适用或可信赖模式。
测量制剂的可及性会因性药物开放的不同第一过程而异。在初期挑战第一过程,可能会不能达到MAbs或PAbs,故一般使用整体上市制造的配体(即生物体体药的靶点)当做关键的化学药品来测定方法矿酸的球蛋白生物体体药(therapeutic protein,TP)的氧浓度。在初期临床检验前研究分析中,重要性IgG Fc组成部分的代用抗原可以用于单克隆抗原药材,虽说仅能测量总酸度(运用靶标后的TP +解离的TPf)。
生态学图标物的降钙素原检测讲解技术
各样体内疾病诊断化学试剂盒在工商业上常用以食用的药物的早前挖掘时间段,也可从同的出售商获得了各样合拼淀粉酶和抗怪物体技术技术工程标签图片物淀粉酶的免疫抗体。尽管怪物体技术技术工程标签图片物的酶联免疫法数据概述数据概述方式与PK方式同类,但这前者范围内会有显然差异。与PK方式类式,怪物体技术技术工程标记物的酶联免疫法数据概述数据概述方式常用以检验工作目标基本材料中怪物体技术技术工程标记物淀粉酶的自由于渗透压值或总渗透压值。夹心式公测文件类型是其主要采用,大多数用以检验怪物体技术技术工程标记物淀粉酶的自由于或总渗透压值。尽管当一款怪物体技术技术工程药拥有压做成用时,必须要自动测量自由于的怪物体技术技术工程标志物蛋白质质量浓度,但定制开发测定法游离的微生物标准物球蛋白的做法有等同于的问题性,很有可能要超额的分离处理步奏。
人源化的或全人源的单克隆抗原或资产重组球核蛋白,做药给与受试者/甲壳绿色后,可介导确立采取该怪物药的抗原,尤其临床上前的甲壳绿色合乐hl8官网性试验中,此类由怪物药介导而确立的抗原基本上被可称抗药抗原(ADA)。免疫系统系统查重方法步骤是查重ADA有无来源于于血清中的一是级查重。不一样的ADA反响,如表位特女性朋友(idiotype vs. nonidiotype,特异与其特女性朋友)和数据(滴度或相对性氧化还原电位),会关系对ADA和怪物药的明确降钙素原检则。根据ADAs会在血渍嵌套循环中与怪物药确立免疫系统系统复合材料物,高氧化还原电位的球核蛋白怪物药就能够要素ADA的查重。
微信备注名:idiotype:免役球淀粉酶(如IgG)可变气门正时地方的团伙结构类型和构象,拥有其抗原活性朋友。
LBA自测做法手段步骤在各方位生物技术分子式的按量剖析方位享用各方位优质。她们在基本都数公司(如比色计或正等轴测图电电学闪光)上,成本低通常情况下很低。当高感召力MAbs使用做LBAs时,LBA做法手段步骤在查重和按量剖析具备于异质性的机质环保中的关键剖析物方位,具备着极度迟钝度和活性聊天。出至学习解析目地,这种做法手段步骤的迟钝度就能够低至每毫升毫左左克的阶段(femtogram/mL)。基本都数LBAs的基本操作软件程序不涉及到试品分开的手段步骤,而应用做LC-MS/MS的按量剖析做法手段步骤则须要。的确,LBA也是有四个优点和缺点,与LC-MS/MS做法手段步骤相对于,LBA做法手段步骤的动态信息的领域较闭塞。即使使用做基础性学习解析的做法手段步骤就能够符合4-6个指數级的动态信息的领域,但使用做规范性学习解析(regulated study)的检验过的做法手段步骤,其按量领域并非仅为2-3个指數级,这是毕竟应该保持着做法手段步骤的稳盈性和好的再现性。
最猛要的不同于是,LBA的性能参数依赖于于所的运行化学采血管的水平和特男人。由此,化学采血管自动生成/选(MAbs或PAbs)是技巧开发建设阶段中的重要性关键步骤,这可以相对用时,3到9三个月一致。当的运行讲解物特男人的化学采血管来驯服阶段目标讲解物时,这类瑕疵对LC-MS/MS技巧也是存在的的。从生物体标识物技巧的度角看来,化学采血管的平行生理作用可造成该技巧的非特男人。由此,激动改进措施开始增加的测验以揭示化学采血管的平行生理作用性和非特男人。
这篇文发展历程了LBA自测软件措施,以及其一般观念的兴起和发展历程,有时候重温了通常用的大碳原子动物深入浅析措施的自测软件文件类型。校园营销原始的LBA自测软件措施演变于1960年,是为测定法胰岛素而開發的牵扯线免役抗体自测软件(radioimmunoassay),LBA自测软件措施的知识基础是也至少要还有一个种球营养物质与感关注的关键深入浅析物有主动做用。在当代的调查室, 酶免役抗体自测软件(enzyme immunoassay)已在比较大方面上所代替了牵扯线性免役抗体自测软件,作为了更好地LBA自测软件措施的安全合乐hl8官网形势。
最后的,今天还简单介绍了其他的多种多样测评格式文件,如竞争者式(competitive)、夹心式(sandwich)和桥接式(bridging),并且其的需求的关键性采血管。最后的,简洁扼要地挑选了LBA测评的方式在球高蛋白怪物药的开发中的选用,并且与其他的怪物了解游戏平台的相当。
自上新时代60年间对胰岛素采取参考值校正到现在,依据与任何微生物体制品团伙通过目的的LBA策略已被常见地用到微生物体制品团伙的参考值深入定性分析。举例子,在蛋清质微生物体制品药激发方式方法流程中,这一些策略为参考值深入定性分析或检则蛋清质提高没事种更准确和生活合理有效的策略。公测实验免疫试剂(MAbs或PAbs)合成/选购是LBA策略激发方式方法流程中的最为关键的方式方法流程,万一选购好好实验免疫试剂,区别公测平舞台上的LBA策略能提高不错节约资源事件和生活代价。
如前所论,另一类个主要的的大碳原子微微海洋动物进行具体阐述网站是高效液相色谱-质谱(LC-MS/MS)。在小碳原子药的微微海洋动物进行具体阐述中,LC-MS/MS工艺是无可非议的霸者,在大碳原子进行具体阐述中,LC-MS/MS的关键性也在不息地提升,特别的是在与LBA工艺以每种方式组合公式接下来。应该确定,微微海洋动物进行具体阐述业内将以后探寻LC-MS/MS在淀粉酶质药的微微海洋动物进行具体阐述中的应用。微微海洋动物进行具体阐述职业有必要证件LC-MS/MS在药建设的全整个过程中,与LBA工艺相较于较,拥有再次出现性(reproducibility)、可移动性(transferability)、信得过性(reliability)和成本预算收益(cost–effectiveness)等地方的明显优势。本品类之后的将简介相关的相关知识,烦请瞩目。
厂家主要来源:动物制作药品厂家
中心句此事疏漏和误解涉及到的导则和数据库的点,请受众讨论和斧正。几乎所有引证的原来消息和数据资料均来于就已投稿科研杂志、关方在线新闻报道等公示黑平台, 不涉及到的所有脱密消息。基准论文论文参考期刊论文的选择考虑的到各样化但也并不应该完整。喜爱受众提拱有社会价值的论文论文参考期刊论文以及开展。
1. Thway TM. Fundamentals of large-molecule protein therapeutic bioanalysis using ligand-binding assays. Bioanalysis (2016) 8(1), 11–17
2. Yalow RS, Berson S A. Immunoassay of endogenous plasma insulin in man. J. Clin. Inv. 39, 1157–1175 (1960).
3. Moss AJ, Dalrymple GV, Boyd CM. Practical Radioimmunoassay. The C.V Mosby, St. Louis, MO, USA (1976).
4. Jaffe BM, Behrman H. Methods of Hormone Radioimmunoassay. Academic, New York, NY, USA, (1979).
5. Travis JC. Fundamentals of RIA and Other Ligand Assays. Scientific Newsletters, Anaheim, CA, USA (1979).
6. Engvall E. Enzyme immunoassay ELISA and EMIT. In: Methods in Enzymology Volume 70. van Vunakis H, Langone J (Eds). Academic, New York, NY, USA, 419–439 (1970).
7. Engvall E, Perlmann P. Enzyme-linked immunosorbent assay (ELISA) quantitative assay of immunoglobulin G. Immunochemistry 8, 871–874 (1971).
8. Jenkins R, et al. “Recommendations for Validation of LC-MS/MS Bioanalytical Methods for Protein Biotherapeutics.” The AAPS Journal1 (2015): 1–16. PMC. Web. 13 Apr. 2016
9. Gao XL, et al. Quantitative analysis of factor P (Properdin) in monkey serum using immunoaffinity capturing in combination with LC–MS/MS. Bioanalysis, March 2016,Vol. 8, No. 5, Pages 425-438 , DOI 10.4155/bio.15.258
10. Zhang YJ, et al. The integration of ligand binding and LC-MS-based assays into bioanalytical strategies for protein analysis. Bioanalysis July 2014 ,Vol. 6, No. 13, Pages 1827-1841 , DOI 10.4155/bio.14.128 (doi:10.4155/bio.14.128)
11. Van Dyke K. Biolumisencence and chemiluminescence: instruments and applications, vol I/II. CRC Press, Baton Roca, FL, USA (1985).
12. Schaap AP, et al. Chemiluminescent substrates for alkaline phosphatase: application to ultrasensitive enzyme-linked immunoassays and DNA probes. Clin. Chem. 35(9), 1863–1864 (1989)
13. Stanley PE, Kricka LJ. Bioluminescence and Chemiluminescence, Current Status. Wiley, New York, NY, USA (1991).
14. Lipman NS, et al. Monoclonal versus polyclonal antibodies: distinguishing characteristics, applications, and information resources. ILAR J. 46(3), 258–68 (2005).
15. DeSilva B, et al. Recommendations for the bioanaltyical method validation of ligand-binding assays to support pharmacokinetic assessments of macromolecules. Pharm. Res. 11, 1885–1900 (2003).
16. Lee J, Ma H. Specificity and selectivity evaluations of ligand binding assay of protein therapeutics against concomitant drugs and related endogenous proteins. AAPS J. 9(2), e164–e170 (2007).
17. Lee JW, et al. Bioanalytical approaches to quantify “total” and “free” therapeutic antibodies and their targets: technical challenges and PK/PD applications over the course of drug development. AAPS J. 13(1), 99–110 (2011).
18. Shih JY, et al. Implementation of a universal analytical method in early-stage development of human antibody therapeutics: application to pharmacokinetic assessment for candidate selection. Bioanalysis 4, 2357–2365 (2012).
19. Lee JW. Method validation and application of protein biomarkers: basic similarities and differences from biotherapeutic. Bioanalysis 1, 1461–1473 (2009).
20. Shankar G, et al. Recommendations for the validation of immunoassays used for detection of host antibodies against biotechnology products. JPBA 15(48), 1267–1281 (2008).
21. Thway TM, et al. Impact of antidrug antibodies in preclinical pharmacokinetic assessment. J. Pharm. Biomed. Anal. 15(3), 856–862. (2013).
22. Cai XY, et al. Challenges of developing and validating immunogenicity assays to support comparability studies for biosimilar drug development. Bioanalysis 4(17), 2169–2177 (2012).