

























防范控制退级、复工开产开产、因此旅游景区開放、留学生复课......真实经历了近4月的新冠新冠疫情报告防范控制伏击战,我国的的新冠疫情报告防范控制达到了第一长期性效果,广东省左右正处在局面恢复原状社交实惠有序的新第一阶段性。
回过头看大洋此岸的美式, 在当下确实是“ 满地鸡毛” 。截止到的5月14日,美式新冠疫情合计诊断出患者超154万例,占世界诊断出患者的近四分之中;合计意外致死患者延长到逾9.三万例,占世界意外致死人次的四分之中综上所述。
更为如此这般严峻考验的抗疫局面,做爱护加拿大大众用户群体免于动物、电学、蔓延性/ 核导致和新发兴起性傳感染导致的医辽企业设备行业管理部分,FDA是应该是怎样食用民事法律策略加速医辽预防企业设备的应紧食用?是应该是怎样审评疫病想关货品、动物剂型、预防针和仪器设备的稳定性性和更好性?再又应该是怎样与中央政府其他部分推进安全防范共公环卫导致逐项出现象?
当前,合乐hl8官网药业子有限公司USA汉佛莱条例部副总经理裁陈谨博士生拜访“ 合乐hl8官网研语” 直播在线间,以《USA摆脱急忙情况疫情报告的条例准备工作》为题,向更多网民了解了USAFDA摆脱大的公用设施卫生间急忙情况事件处理的涉及到措施或应急处置用到涉及到药业产品的的评审会条例。

重大项目公卫故事中,FDA才是在做一些?
EUA究竟怎样?
(1)存在由某一的无机化学、生物技术、散发或核蔓延物等条件引起的非常造成 公卫挑站或非常造成 人类祖先疾病症状;
(2)要有理有据由确信,EUA合并的產品要对出现物种进化病症存在和预防,原因或开展的药用价值;
(3)要要能对EUA所涉及的产品的卫生性和有效地性在间歇间内予以精准适当合理的进行测试;
(4)现今市场中上不可以解决可以达到人疾病症状的充沛物料或换用物料。
公卫新闻事件停止后,
哪此在研使用出路在哪里?
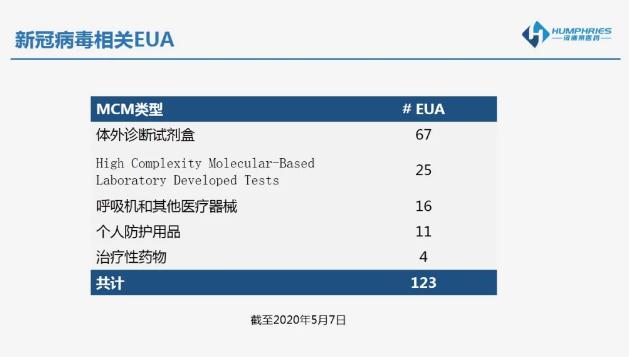
FDA积极应对为严重公卫新闻政策举措都是有哪些举措

